كما ذكرنا سابقًا ، العناصر القابلة للاحتراق في الوقود هي الكربون C ، الهيدروجين H والكبريت القابل للاحتراق المتطاير S. يمكن تمثيل الاحتراق الأولي بالمعادلات التالية:
ج + 0 2 = C0 2 ؛ 2H 2 +0 2 \ u003d 2H 2 0 ؛ س + 0 2 = س 0 2. (6)
في عملية احتراق العناصر القابلة للاحتراق ، يتم إطلاق الوقود أثناء احتراق 1 كجم:
كربون - 7854 كيلو كالوري / كغ
الهيدروجين - 34180 (يخضع لتكوين الماء وليس بخار الماء ، وإلا - 28905 كيلو كالوري / كجم)
إذا افترضنا أن العناصر التي يتكون منها الوقود موجودة فيه في شكل خليط ميكانيكي ، فيمكن حساب القيمة الحرارية للوقود كمجموع بناءً على معلومات حول احتراق العناصر القابلة للاحتراق.
ومع ذلك ، فإن تحديد القيمة الحرارية بهذه الطرق يعطي تباينًا كبيرًا مع القيمة الحرارية الفعلية التي تحددها طريقة قياس السعرات الحرارية. هذا يرجع إلى حقيقة أنه لا يمكن اعتبار الوقود مزيجًا ميكانيكيًا من العناصر الفردية. جزيئات الوقود لها بنية معقدة للغاية ، وفي عملية الاحتراق ، يحدث التحلل الكيميائي للجزيئات مع إنفاق الحرارة لهذه العمليات.
وهكذا ، بمعرفة التركيب الأولي للوقود ، لا يمكن تحديد قيمته الحرارية إلا تقريبًا بواسطة الصيغ التجريبية ؛ من بين هؤلاء ، ينتمي الأكثر دقة إلى D.I Mendeleev ويتم التعبير عنه على النحو التالي:
Q r in \ u003d 81C P + 300H P - 26 (O r - S r l) kcal / kg. (7)
يتم التحديد المباشر للقيمة الحرارية عن طريق حرق عينة من الوقود في جو أكسجين. لهذه الأغراض ، يتم استخدام ما يسمى بالقنبلة المسعرية ، وهي وعاء سميك الجدران يوضع فيه الوقود ويتم حقن الأكسجين بضغط 25-30 ضغط جوي.
تبلغ سعة القنبلة (الشكل ب) حوالي 300 سم وهي مصنوعة من الفولاذ المقاوم للأحماض. يوجد في غطاء القنبلة صمامات لتزويد الأكسجين وإطلاق الغازات المحترقة. يتم توفير الأكسجين من خلال أنبوب في قاع القنبلة ؛ تتم إزالة الغازات من الأعلى. يتم توصيل قضيب بغطاء القنبلة ، حيث يتم توصيل كوب بلاتيني أو كوارتز ، وتوضع عينة فيه. وقود صلبأو صب السائل. القضيب والأنبوب الذي يمد شكل الأكسجين دائرة كهربائيةبالوقود ، والقضيب معزول كهربائيًا عن جسم القنبلة. يمر تيار كهربائي عبر الدائرة. الدائرة مغلقة بسلك فولاذي رفيع.
يتم أخذ عينة من الوقود الصلب تساوي 0.8-1.5 جم ، سائل - 0.6-0.8 جم. غالبًا ما يتم تشكيل فحم حجري من عينة من الوقود الصلب ، حيث يتم ضغط شبكة الإغلاق في سلك الإشعال ، والذي يحترق عند المرور من خلاله هو - هي التيار الكهربائيالجهد 12-15 فولت. السلك يحترق ويشعل النار في عينة الوقود. يتم حرق الوقود غير المسبوك (أنثراسايت ، الفحم الخالي من الدهون ، الصخر الزيتي ، المخلفات البؤرية) في شكل مسحوق. سلك الإشعال مثني بحيث يكون ملامسًا للوقود (مسحوق الوقود الصلب أو الوقود السائل).
القنبلة مغمورة في وعاء مملوء بالماء وتبلغ سعته 2000-2500 سم 3. يتم وضع هذا المسعر ، بدوره ، في علبة معدنية ذات جدران مزدوجة ، ويمتلئ الفراغ بينهما بالماء. تحمي هذه الحالة المسعر إلى حد كبير من التبادل الحراري مع البيئة.
تم تجهيز المسعر بأدوات تحريك خاصة يتم تشغيلها بواسطة محرك كهربائي وتستخدم لموازنة درجة حرارة الماء.
يجب عزل غرفة قياس السعرات الحرارية ، بحيث تكون النوافذ مواجهة للشمال قدر الإمكان لتجنب التعرض لأشعة الشمس.
بعد وضع عينة من الوقود في القنبلة ودخول الأكسجين بضغط يصل إلى 25-30 ضغط جوي ، يمر تيار عبر الدائرة الكهربائية ، وسلك الإشعال وتحترق العينة.
تسخن الحرارة المنبعثة ماء المسعر ؛ لوحظ زيادة في درجة حرارة الماء بواسطة مقياس حرارة خاص بدقة 0.001 درجة.
يتم عرض أقسام مقياس الحرارة من خلال أنبوب بصري متصل بإحكام بحامل ثلاثي الأرجل ، مما يستبعد احتمال وجود أخطاء فردية معروفة في تحديد علامة الزئبق الدائمة.
في الوقود وفي أسطوانة الأكسجين ، حيث يدخل الأخير إلى القنبلة ، توجد كمية معينة من النيتروجين ، مما يساهم في تكوين حمض النيتريك في القنبلة ؛ بنفس الطريقة ، يحترق الكبريت المتطاير في وجود الماء إلى حمض الكبريتيك. يكون تكوين هذه الأحماض مصحوبًا بإطلاق حرارة ، والتي يجب حسابها وطرحها من القيمة الحرارية الناتجة ، حيث لا تتشكل هذه الأحماض في الممارسة التشغيلية لاحتراق الوقود. يتم الحصول على الماء ، الذي يشكل الأحماض ، في القنبلة بسبب تكثيف بخار الماء ؛ لضمان حل الأحماض تمامًا ، يتم سكب 10 سم 3 من الماء المقطر في القنبلة.
أثناء احتراق عينة من الوقود ، يتم امتصاص الحرارة ليس فقط بواسطة ماء المسعر ، ولكن أيضًا عن طريق التركيب بالكامل ، والذي يتكون من وعاء مسعر مع الماء الذي يُسكب فيه ، ومحرك ، ومقياس حرارة ، وقنبلة بها محتوياته. تختلف السعات الحرارية للأجزاء الفردية ، لذلك يتم معايرة القنبلة مبدئيًا عن طريق حرق مادة فيها ، تكون قيمتها الحرارية معروفة بدقة ولا تتغير. في هذه التجربة ، يتم تحديد المكافئ المائي للقنبلة ، أي يتم استبدال امتصاص الحرارة لجميع الأجزاء المدرجة في التركيب بامتصاص الحرارة لوزن مكافئ من الماء. عادةً ما تُستخدم عينة من حمض البنزويك كمادة تُحرق أثناء المعايرة.
المسعر في الغرفة ، حتى بدون حرق الوقود ، اعتمادًا على ظروف درجة الحرارة ، سيعطي أو يتلقى الحرارة بيئة. لذلك ، فإن الاختلاف في درجة الحرارة الموجود في الفترة من بداية الاحتراق إلى نهاية ارتفاع درجة حرارة الماء في المسعر لن يميز بعد القيمة الحرارية للوقود. من الضروري إدخال تصحيح للتبادل الحراري للجهاز مع البيئة ، لأنه خلال هذا الوقت ، يمكن أن يعطي أو يستقبل الحرارة بدوره. عن طريق التسجيل المنتظم لدرجة حرارة الماء لبعض الوقت قبل التجربة وأثناء التجربة وبعدها يمكن الحصول على هذا التصحيح. يتم تحديد التصحيح على أساس تحديد حجم التغير في درجة حرارة الماء في المسعر فقط بسبب التعرض للبيئة. بمعرفة وزن سلك الإشعال وقيمته الحرارية ، يمكن إجراء تصحيح لحرق السلك.
نتيجة لذلك ، يتم تحديد القيمة الحرارية لوقود القنبلة بالصيغة التالية:
Q ب \ u003d K [(t n + h) - (t o + h o) + t] - ∑qv / a (8)
حيث Q b هي القيمة الحرارية لقنبلة العينة التحليلية بالكيلو جرام ؛
أ هو وزن عينة الوقود بالجرام ؛
K هو المكافئ المائي للمسعر بالجرام ؛
t n - درجة حرارة الماء النهائية بعد احتراق العينة بالدرجات ؛
t o - درجة حرارة الماء الأولية قبل الاحتراق بالدرجة ؛
h و h o عبارة عن تصحيحات لقراءات مقياس الحرارة (وفقًا لمخططات المعايرة) بالدرجات ؛
ب هو وزن سلك الإشعال بالجرام ؛
q هي حرارة احتراق المصهر ؛ مقبول: للأسلاك الفولاذية - 1600 كالوري / غرام ، للنيكل - 775 كالوري / غرام ، لخيوط الخياطة الورقية - 4000 كالوري / غرام ؛
∑qv - مجموع حرارة احتراق المصهر عند استخدام سلك به خيط في البراز ؛
Δt - تصحيح التبادل الحراري للجهاز مع البيئة في درجة.
يدخل النيتروجين إلى القنبلة المسعرية مع الأكسجين من الأسطوانة ، وكذلك من عينة الوقود. نتيجة لأكسدة النيتروجين بالأكسجين في وجود الماء ، يتكون حمض النيتريك.
بناءً على نتائج سنوات عديدة من التجارب ، اقترح A. I.Karelin معادلة التصحيح التجريبية التالية لتكوين حمض النيتريك في ظل ظروف معينة:
س N \ u003d 0.0015Q 6 كال / ز. (تسع)
تمت الموافقة على التعديل من قبل GOST ذات الصلة.
عندما يتم حرق الكبريت القابل للاشتعال في الوقود ، يتشكل SO 2 ، وفي وجود الماء يتشكل حمض الكبريتيك H 2 S0 4. لكل جرام من الكبريت المتطاير في الوقود ، يؤدي تكوين حامض الكبريتيك إلى إطلاق 2250 كالوري ، أو 1٪ -22.5 كالوري. وبالتالي ، يمكن التعبير عن تصحيح تكوين حامض الكبريتيك على النحو التالي:
Qs = 22.5S لتر كالوري / جم (10)
بطرح قيمة السعرات الحرارية التي تم الحصول عليها من القنبلة ، تكلفة الحرارة لتكوين الأحماض ، يتم تحديد القيمة الحرارية للوقود وفقًا لما يسمى الحد الأعلى:
Q in \ u003d Q b - 0.0015Q b - 22.5S l cal / g. (أحد عشر)
إذا تم تحديد القيمة الحرارية لوقود العمل ، فيمكنك الكتابة
Q p b \ u003d Q p b - 0.0015Q p b -22.5 S p l kcal / kg. (12)
عند التحديد التجريبي للقيمة الحرارية للوقود عن طريق قياس المسعر ، يتكثف بخار الماء الناتج عن تفاعل الاحتراق على الجدران الباردة نسبيًا للقنبلة ، ويعيد الحرارة الكامنة للتبخر. لذلك ، فإن القيمة الحرارية للوقود ، المحددة في القنبلة المسعرية ، ستكون أعلى من كمية الحرارة التي يمكن تحقيقها في ظل الظروف العملية لاحتراق الوقود في أفران الغلايات أو الأفران.
يمكن تحديد العلاقة بين القيمة الحرارية عند الحد الأعلى والأدنى ، مع الأخذ في الاعتبار فقدان الحرارة الكامنة للتبخر ، على النحو التالي.
يتم حساب كمية وزن بخار الماء المتكون نتيجة احتراق الهيدروجين بضرب وزن الهيدروجين في 1 كجم من الوقود (H p / 100) [انظر. الصيغة (1)] ، بمقدار 9 ، لأن احتراق 1 كجم من الهيدروجين ينتج 9 كجم من الماء. يضاف هذا إلى وزن الماء (W p / 100) الموجود في الوقود ويتبخر أثناء احتراقه. يجب أن تؤخذ القيمة الرقمية للحرارة الكامنة للتبخر في الاعتبار الضغط الجزئي لبخار الماء في غازات العادم ويتم تقريبها إلى 600 كيلو كالوري / كجم.
القيمة الحراريةيتم تحديد وقود العمل من خلال الصيغة
Q p n \ u003d Q p b -600 (9H · p + W · p / 100) \ u003d Q p b -6 (9H · p + W · p) kcal / kg. (13)
يمكن أيضًا تحديد القيمة الحرارية للوقود الغازي في القنبلة ، ولكن من الناحية الفنية يتبين أن هذه الطريقة معقدة ، وغالبًا ما تستخدم المسعرات المعدلة خصيصًا لاحتراق الغاز في البحث.
يتم إجراء التحويل المتبادل للقيمة الحرارية لتكوين وقود إلى آخر بشكل مشابه لتحويل التكوين الأولي ، فقط من الضروري مراعاة استهلاك الحرارة لتبخر الماء.

![]()
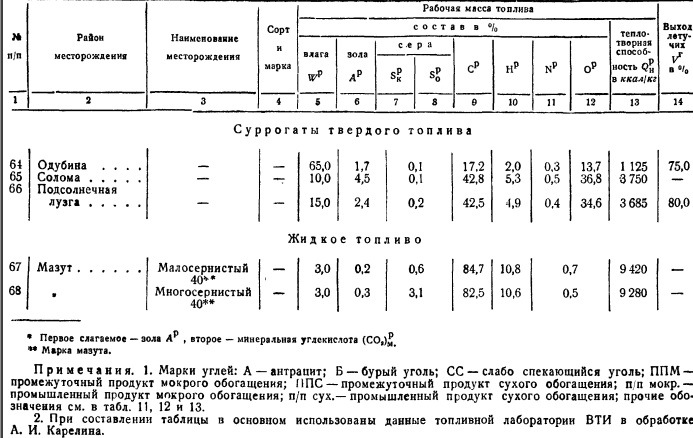
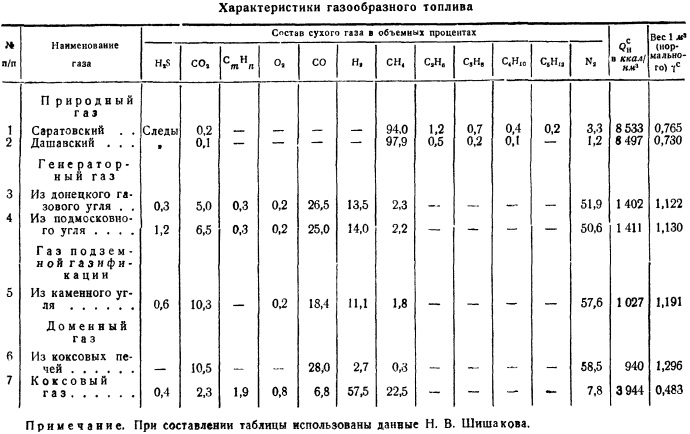
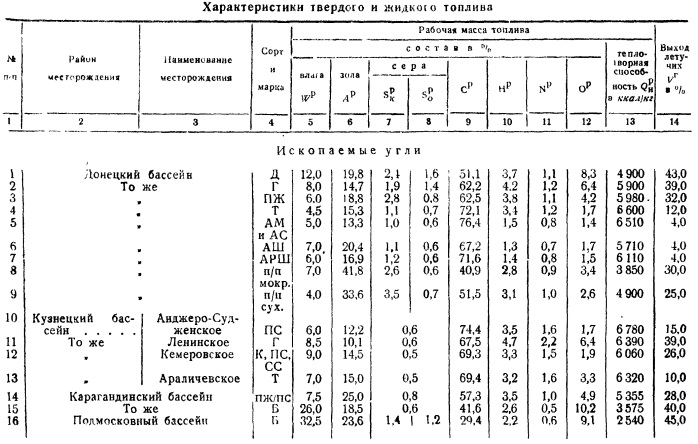
قنبلة مسعرية. ستتم مناقشة طرق أخذ عينة وقود متوسطة بالتفصيل في الفقرة 6. من الضروري فقط ملاحظة أن تكوين معظم أنواع الوقود متغير للغاية حتى بالنسبة لنفس موقع التعدين ، ودرز الفحم ، والمنجم ، والمستنقعات ، وما إلى ذلك ، لذلك ، لتوصيف رواسب الوقود ، من الضروري إجراء دراسات عديدة لعينات متوسطة واستخدامها للحكم على بعض الأرقام المتوسطة لتكوين الوقود ، والقيمة الحرارية لكتلته القابلة للاحتراق ، وما إلى ذلك. هذه المادة يمتلكها الوقود الكيميائي. المختبرات ، التي لم يتم تنظيمها حتى الآن إلا بواسطة مختبر VTI ، الذي ينشر بشكل دوري الخصائص النوعية للوقود. بناءً على هذه البيانات ، الجدول. 2 ، والذي يوضح تكوين الكتلة العاملة بمتوسط عدد نموذجي للرماد وتلوث الرطوبة. يتم إعطاء القيمة الحرارية الصافية لهذه الظروف المتوسطة.
إذا كان يجب ، في ظروف معينة ، أخذ الصابورة الخارجية للوقود (الرماد والرطوبة) بشكل مختلف عن المتوسط ، فمن السهل إعادة حساب الكتلة القابلة للاحتراق أولاً ، ثم للظروف الجديدة.
عند التصميم ، يمكنك أخذ التركيبة والقيمة الحرارية وفقًا للجدول. 2. عند إجراء التجربة ، يتم أخذ عينة متوسطة ثم فحصها في معمل كيميائي ، حيث يتم تحديد كل من التركيب الأولي للوقود وقيمته الحرارية.
كمية الحرارة في السعرات الحرارية الناتجة عن 1 كلغوقود صلب أو سائل أو 1 م 3الغاز أثناء الاحتراق. ت. ر. يتم تحديده في أجهزة خاصة تسمى. القنابل المسعرية والمسعرات. عندما يتم حرق الوقود في هذه الأجهزة ، يتم نقل بخار الماء الناتج عن الاحتراق إلى الحالة السائلة ، وبالتكثيف ، يتخلى عن حرارته تمامًا. وفي الوقت نفسه ، في التركيبات الحرارية ، نظرًا لحقيقة أن درجة حرارة غازات العادم أعلى دائمًا من درجة حرارة التكثيف ، يظل الماء الناتج عن الاحتراق في حالة بخار ، وبالتالي ، لا يمكن لحرارة التبخر الموجودة في حرارة الاحتراق يستخدم. وبالتالي. arr. ، لأغراض عملية ، تكون حرارة الاحتراق أكثر دلالة دون مراعاة حرارة التبخر أو ، بشكل أدق ، حرارة تكثيف الماء. هذه الحرارة ، على عكس حرارة الاحتراق التي تم الحصول عليها في قنبلة مسعرية (أعلى T. s. t.) ، تسمى. انخفاض T. مع. تي ؛ إنها تساوي الأعلى ناقص 600 (9 ح+دبليو) / 100 أين و ث-النسبة المئوية للهيدروجين والرطوبة في وقود معين. في الولايات المتحدة ، يتم إدخال أعلى T. s في جميع الحسابات. ر ، في اتحاد الجمهوريات الاشتراكية السوفياتية وأوروبا الغربية - الأدنى ؛ في الآونة الأخيرة ، ومع ذلك ، كان هناك اتجاه لصالح الانتقال إلى T. s أعلى. ت.
القاموس الفني للسكك الحديدية. - م: دار نشر السكك الحديدية للنقل العام. N.N.Vasiliev، O.N. Isaakyan، N. O. Roginsky، Ya. B. Smolyansky، V. A. Sokovich، T. S. Khachaturov. 1941 .
شاهد ما هو "HEALTH CAPACITY OF FUEL" في القواميس الأخرى:
كمية الحرارة المنبعثة أثناء الاحتراق 1 كجم. صلبة أو 1 متر مكعب وقود غازي. تعتمد القيمة الحرارية لكل نوع من أنواع الوقود على: مكوناته القابلة للاحتراق: الكربون ، والهيدروجين ، والكبريت المتطاير القابل للاحتراق ، وما إلى ذلك ؛ وكذلك من محتواها من الرماد و ... ... مفردات مالية
القيمة الحرارية للوقود- - [Ya.N. Luginsky، MS Fezi Zhilinskaya، YuS Kabirov. القاموس الإنجليزي الروسي للهندسة الكهربائية وصناعة الطاقة ، موسكو ، 1999] موضوعات الهندسة الكهربائية ، المفاهيم الأساسية EN كفاءة الوقود ...
القيمة الحرارية للوقود- 34 قيمة حرارية للوقود: إجمالي كمية الطاقة التي يمتلكها الوقود ، ويطلقها في ظل ظروف منظمة. ملاحظة: يتم التعبير عن القيمة الحرارية للوقود بالميغاجول لكل كيلوغرام (MJ / kg) ، بالميغاجول لكل ... ...
- ... ويكيبيديا
القيمة الحرارية الصافية للوقود المستخدم للتدفئة الإضافية- - [أ.س. غولدبرغ. قاموس الطاقة الإنجليزية الروسية. 2006] موضوعات الطاقة بشكل عام القيمة الحرارية الصافية لوقود التدفئة الإضافي EN ... دليل المترجم الفني
كمية الحرارة ، التي يتم تقليلها إلى وحدة وزن من حجم الوقود ، تنطلق أثناء الاحتراق عند ضغط ثابت قدره 101320 باسكال في الأكسجين وتبريد نواتج الاحتراق إلى درجة الحرارة المحيطة. ملاحظات 1. تحتوي هذه القيمة على مخفي ... ... دليل المترجم الفني
القيمة الحرارية الإجمالية للوقود- 3.1.5 القيمة الحرارية الإجمالية للوقود (القيمة الحرارية الإجمالية): مقدار الحرارة ، مخفضًا إلى وحدة وزن من حجم الوقود ، ويتم إطلاقه أثناء الاحتراق عند ضغط ثابت قدره 101320 باسكال في الأكسجين وتبريد نواتج الاحتراق إلى .. .... قاموس - كتاب مرجعي للمصطلحات المعيارية والتقنية
القيمة الحرارية- 3.1.1 مقدار القيمة الحرارية للحرارة الناتجة عن احتراق وحدة حجم أو كتلة لعينة في ظل ظروف محددة في هذا المعيار ، يتم التعبير عن القيمة الحرارية بالجول لكل 1 كجم (J / كجم) ... ... قاموس - كتاب مرجعي للمصطلحات المعيارية والتقنية
القدرة الحرارية ، القدرة على توليد الحرارة. القيمة الحرارية هي أساس تشغيل أي محرك حراري. يتم تحويل الحرارة المنبعثة أثناء احتراق الوقود إلى طاقة مفيدة ، على سبيل المثال ، تقوم بتحريك مكابس قاطرة ... ... القاموس الموسوعي العلمي والتقني
القيمة الحرارية للوقود الهيدروكربوني- إجمالي كمية الطاقة التي يمتلكها الوقود الهيدروكربوني الطبيعي ، والتي يتم إطلاقها في ظل ظروف منظمة ...
الأكثر شيوعا تفاعلات كيميائيةتستخدم لتوليد الحرارة هي تفاعلات احتراق. تسمى الطاقة المنبعثة أثناء احتراق الوقود أو الطعام القيمة الحرارية(سعرات حراريهنظرًا لأن جميع تفاعلات الاحتراق طاردة للحرارة ، فمن المعتاد الإشارة إلى القيمة الحرارية بدون علامة سلبية. أيضًا ، نظرًا لأن الوقود والمواد الغذائية عادة ما تكون مخاليط ، يتم الإبلاغ عن قيمتها الحرارية لكل جرام وليس لكل مول. على سبيل المثال ، القيمة الحرارية لأوكتان C 8 H 18 ، أحد مكونات البنزين ، هي الحرارة المنبعثة أثناء احتراق 1 جرام من هذه المادة:
2C 8 H 18 (l.) + 25O 2 (g.) → 16CO 2 (g.) + 18H 2 O (g.) (1.17)
لاحظ أنه في هذا التفاعل ، يعتبر الماء ، وهو أحد المنتجات ، كمادة غازية. الحقيقة هي أنه في ظروف احتراق الأوكتان ، يجب أن يتبخر الماء. التغيير في المحتوى الحراري لتفاعل معين = - 10920 كيلو جول. نظرًا لأن كل مول من C 8 H 18 يحتوي على كتلة 114 جم ، فإن القيمة الحرارية للأوكتان هي 47.9 كيلو جول / جم:
(10920 kJ / 2 mol C 8 H 18) × (1 mol C 8 H 18/114 g C 8 H 18) \ u003d 47.9 kJ / g C 8 H 18
وفقًا للقانون الأول للديناميكا الحرارية ، يجب ألا تعتمد القيمة الحرارية لأي مادة على كيفية تفاعلها أو مكان تفاعلها ، بشرط أن تظل نواتج التفاعل دون تغيير. لذلك ، غالبًا ما يستخدم مقياس السعرات الحرارية للقنبلة لقياس القيمة الحرارية (محتوى السعرات الحرارية) للأطعمة. لا شك أن هذه الطريقة أبسط بكثير من قياس كمية الحرارة المنبعثة في محرك السيارة أو في جسمنا.
السعرات الحرارية الغذائية
تأتي معظم الطاقة التي يحتاجها الجسم من الكربوهيدرات والدهون. في عملية الهضم ، تتحلل الكربوهيدرات إلى جلوكوز C 6 H 12 O 6. الجلوكوز قابل للذوبان في الدم وغالبًا ما يشار إليه باسم سكر الدم. ينتقل عن طريق مجرى الدم إلى خلايا الجسم ، حيث يتفاعل مع O 2 على عدة مراحل ، ويتحول في النهاية إلى CO 2 (g.) و H 2 O (l.) مع إطلاق الطاقة:
C 6 H 12 O 6 (tv.) + 6O 2 (g.) → 6CO 2 (g.) + 6H 2 O (l.) \ u003d - 2816 kJ
يحدث تحلل الكربوهيدرات بسرعة ، لذلك تدخل طاقتها إلى الجسم على الفور. ومع ذلك ، فإنه يخزن كمية صغيرة جدًا من الكربوهيدرات. يبلغ متوسط محتوى الكربوهيدرات من السعرات الحرارية 17 كيلو جول / جرام (4 كيلو كالوري / جرام).
مثل الكربوهيدرات ، يتم تحويل الدهون أيضًا إلى CO 2 و H 2 O نتيجة لعملية التمثيل الغذائي (فهي تعطي نفس المنتجات عند حرقها في قنبلة مسعرية). على سبيل المثال ، يحدث احتراق إستيارين دهني نموذجي C 57 H 110 O 6 وفقًا للمعادلة:
2C 57 H 110 O 6 (صلب) + 163O 2 (g.) → 114CO 2 (g.) + 110H 2 O (l.)
= - 75520 كيلو جول
يتم تخزين الطاقة الكيميائية للطعام ، والتي لا تُستخدم للحفاظ على درجة حرارة الجسم أو نشاط العضلات ، أو في النهاية لإعادة ترتيب ذرات الطعام في خلايا الجسم ، على شكل دهون.
1.3 الجدول
محتوى السعرات الحرارية وتكوين بعض المنتجات الشائعة
| منتج غذائي | تكوين تقريبي ، % | سعرات حراريه | |||
| السناجب | الدهون | الكربوهيدرات | كيلوجول / ز | كيلو كالوري / ز | |
| البازلاء الخضراء | 1,9 | - | 7,0 | 1,5 | 0,38 |
| الفول السوداني | 5,5 | ||||
| لبن | 3,3 | 4,0 | 5,0 | 3,0 | 0,74 |
| جعة* | 0,3 | 1,2 | 1,8 | 0,42 | |
| فدج (دسم) | 4,4 | ||||
| النقانق | - | 3,6 | |||
| جبن شيدر | 4,7 | ||||
| خبز (أبيض) | 2,8 | ||||
| التفاح (طازج) | 0,4 | 0,5 | 2,5 | 0,59 | |
| بيض | 0,7 | 1,4 | |||
| * تحتوي البيرة عادة على 3.5٪ من الإيثانول الذي يحتوي على نسبة من السعرات الحرارية. |
هناك سببان على الأقل لكون الدهون ملائمة لتخزين الطاقة الزائدة في الجسم: 1) أنها غير قابلة للذوبان في الماء ، مما يسمح لها بالتراكم في الجسم ؛ 2) تطلق الدهون طاقة أكبر لكل جرام من البروتينات أو الكربوهيدرات ، مما يجعلها المصدر الأكثر كفاءة للطاقة. يبلغ متوسط محتوى الدهون من السعرات الحرارية 38 كيلو جول / جرام (9 كيلو كالوري / جرام).
ينتج عن استقلاب البروتينات في الجسم إطلاق طاقة أقل من الاحتراق في قنبلة مسعرية ، لأنها تعطي نواتج تفاعل مختلفة. تحتوي البروتينات على النيتروجين ، والذي يتم إطلاقه في مسعر القنبلة مثل N 2. يُفرز هذا النيتروجين من الجسم بشكل رئيسي على شكل يوريا CH 4 N 2 O. يستخدم الجسم البروتينات بشكل أساسي ك مواد البناءلجدران الخلايا في مختلف الأعضاء والجلد والشعر والعضلات وما إلى ذلك. في المتوسط ، يطلق التمثيل الغذائي للبروتين 17 كيلو جول / جم (4 كيلو كالوري / جم).
يتم عرض محتوى السعرات الحرارية لبعض المنتجات الأكثر شيوعًا في الجدول. 1.3
تمرين 1.10
تشير التقديرات إلى أن الشخص الذي يركض بمتوسط وزن يستهلك طاقة تبلغ 100 كالوري لكل كيلومتر. كم عدد النقانق التي تحتوي على محتوى من السعرات الحرارية يسمح لك بالركض لمسافة 3 كيلومترات؟
المحلول:تذكر أن السعرات الحرارية للطعام تعادل 1 كيلو كالوري. يتطلب الجري لمسافة 3 كيلومترات إنفاق طاقة 300 سعرة حرارية ، أي 300 كالوري العدد المطلوب من النقانق = 300 كيلو كالوري (1 جرام نقانق / 3.6 كيلو كالوري) = 83 جرام نقانق. وبالتالي ، لتشغيل 3 كيلومترات ، يكفي تناول 100 غرام من النقانق.
تعتمد متطلبات الجسم من الطاقة بشكل كبير على عوامل مثل وزن الجسم والعمر ونشاط العضلات. في المتوسط ، يحتاج الشخص البالغ حوالي 6300 كيلوجول (1500 كيلو كالوري) يوميًا إذا كان مستريحًا في غرفة دافئة. عند القيام بعمل متوسط الشدة ، تزداد احتياجات الطاقة إلى ما يقرب من 10000-13000 كيلو جول (2500-3000 كيلو كالوري) في اليوم. هذا يتوافق تقريبًا مع كمية الطاقة التي يستهلكها مصباح إضاءة 100 واط في 24 ساعة.
السعة الحرارية للوقود
في الجدول. 1.4 الخصائص مقارنة أنواع مختلفةالوقود. لاحظ أن القيمة الحرارية للوقود تزداد مع زيادة المحتوى النسبي للكربون أو الهيدروجين فيها. على سبيل المثال ، القيمة الحرارية للفحم القار أعلى من قيمة الخشب لأن الفحم يحتوي على المزيد من الكربون.
يتم استدعاء الفحم والنفط والغاز الطبيعي ، والتي تعد حاليًا مصادرنا الرئيسية للطاقة معادن قابلة للاشتعال.من المفترض أنها تشكلت منذ ملايين السنين نتيجة تحلل النباتات والحيوانات. يتم إنفاقها جميعًا حاليًا بشكل أسرع من تراكمها الإضافي. غاز طبيعييتكون من الهيدروكربونات الغازية (مركبات الكربون والهيدروجين). تعبير غاز طبيعييختلف ، لكنه في الغالب يحتوي على الميثان CH 4 مع إضافات صغيرة من الإيثان C 2 H 6 ، البروبان C 3 H 8 والبيوتان C 4 H 10. زيتعبارة عن خليط سائل من مئات المركبات المختلفة. معظمها عبارة عن هيدروكربونات ، والباقي عبارة عن مركبات عضوية بشكل أساسي تحتوي على الكبريت أو النيتروجين أو الأكسجين. فحمهي مادة صلبة تحتوي على هيدروكربونات ذات وزن جزيئي كبير ، بالإضافة إلى مركبات الكبريت والأكسجين والنيتروجين. وجود الكبريت في الفحم والنفط له أهمية عظيمةعند مناقشة مشكلة تلوث الهواء.
الجدول 1.4
القيمة الحرارية وتكوين بعض أنواع الوقود الشائعة
الهيدروجين H 2 وقود واعد للغاية ، لأنه يحتوي على قيمة حرارية عالية جدًا ، وعندما يتم حرقه يتكون الماء فقط ، لذلك فهو وقود "نظيف" لا يسبب تلوث الهواء. ومع ذلك ، فإن استخدامه على نطاق واسع كمصدر للطاقة يعوقه حقيقة أن الطبيعة تحتوي على كمية قليلة جدًا من H2 في شكل حر. يتم إنتاج معظم الهيدروجين عن طريق تحلل الماء أو الهيدروكربونات. يتطلب هذا التحلل استهلاكًا للطاقة ، وفي الممارسة العملية ، بسبب فقد الحرارة ، يجب إنفاق المزيد من الطاقة لإنتاج الهيدروجين أكثر مما يمكن الحصول عليه مع الاستخدام اللاحق للهيدروجين كوقود. ومع ذلك ، إذا كان من الممكن إنشاء مصادر طاقة كبيرة ورخيصة نتيجة لتطور التكنولوجيا للحصول على الطاقة النووية أو الشمسية ، فيمكن استخدام جزء منها لإنتاج الهيدروجين. يمكن بعد ذلك استخدام هذا الهيدروجين كناقل مناسب للطاقة. من المربح اقتصاديًا نقل الهيدروجين عبر خطوط أنابيب الغاز الحالية بدلاً من نقل الكهرباء ؛ الهيدروجين مناسب لكل من النقل والتخزين. لأن التكنولوجيا الصناعية الحديثة تعتمد على الوقود القابل للاشتعال ، يمكن للهيدروجين أن يحل محل النفط والغاز الطبيعي لأن هذين الوقودين يصبحان مستنفدين وأكثر تكلفة.
1.8 استهلاك الطاقة: الاتجاهات والآفاق
ينخفض أعلى متوسط استهلاك يومي للطاقة للفرد في العالم ويبلغ حوالي 1.3 10 6 kJ. هذه الكمية من الطاقة أكبر بحوالي 100 مرة من احتياجاتنا من الطاقة في الطعام. يتزايد استهلاك الطاقة كل عام ، كما هو موضح في الشكل. 1.6 في الوقت الحاضر ، ما يقرب من 30 ٪ من السنوي
محطات الطاقة الكهرومائية وأكثر بقليل من 2٪ - محطات الطاقة النووية. أكبر مشكلة في استخدام الوقود الأحفوري هي أننا ، في النهاية ، سنستنفده تمامًا. عند القيام بذلك ، سيتعين علينا الاعتماد على مصادر باهظة الثمن بشكل متزايد لهذه الأنواع من الوقود.
مصادر الطاقة في المستقبل
وفقًا لبعض التقديرات ، بحلول نهاية القرن العشرين ، يجب استنفاد الاحتياطيات الحالية من النفط والغاز الطبيعي تمامًا ، ما لم تظهر مصادر أخرى للطاقة أو لا ينخفض استهلاك الفرد. هذا يحدد الاهتمام الكبير في إنشاء مصادر طاقة جديدة. يتم حاليًا تركيز الكثير من الجهود على استكشاف إمكانيات استخدام الطاقة النووية والشمسية وتطوير طرق لاستخدام الفحم بشكل أكثر كفاءة. هناك أيضًا اهتمام باستخدام الطاقة الحرارية الأرضية (الطاقة الحرارية القادمة من أحشاء الأرض) وطاقة الرياح والمد البحري. يتوقع الخبراء أن كل من مصادر الطاقة الثلاثة هذه يمكن أن تقدم مساهمة صغيرة ولكن مهمة في توازن الطاقة الكلي ، ولكن بشكل عام لن يكون لها تأثير حاسم في المستقبل المنظور ، وبالتالي فإننا لا نناقشها بمزيد من التفصيل. هنا سوف نتحدث بإيجاز فقط عن مشاكل استخدام الفحم والطاقة الشمسية.
تتجاوز احتياطيات الفحم تلك الموجودة في جميع أنواع الوقود الأحفوري الأخرى ؛ تمثل 80٪ من احتياطي الوقود الأحفوري في الولايات المتحدة و 90٪ في جميع أنحاء العالم. ومع ذلك ، فإن استخدام الفحم يواجه عددًا من المشاكل. من بين جميع أنواع الوقود ، يسبب الفحم معظم تلوث الهواء. غالبًا ما يكون إنتاجه مكلفًا وغير آمن. قد توجد رواسب الفحم بعيدًا عن مناطق استهلاكه ؛ على سبيل المثال ، في الولايات المتحدة ، تقع معظم رواسب الفحم الغني غير المستغلة في الجزء الغربي من البلاد ، ويتركز مستهلكو الطاقة في الغالب على طول الساحل الشرقي ؛ نقل الفحم لمسافات طويلة يزيد من تكلفته. يجادل بعض الخبراء بأنه يمكن استخدام الفحم بشكل أكثر كفاءة إذا تم تحويله إلى غاز ، وهو ما يسمى الغاز التخليقي ("غاز التخليق"). يمكن لعملية التحويل إزالة الكبريت من الفحم ، مما يقلل من تلوث الهواء أثناء الاحتراق اللاحق للغاز التخليقي. يسهل نقل غاز Syngas عبر الأنابيب ويمكنه تجديد إمدادات الغاز الطبيعي المتضائلة. يتطلب تغويز الفحم إضافة الهيدروجين إليه. للقيام بذلك ، يتم سحق الفحم في الغبار ، والذي يتم معالجته بالبخار المحمص. يحتوي المنتج على خليط من CO و H 2 و CH 4 ويمكن استخدام كل هذه المواد كوقود. ومع ذلك ، يتم اختيار شروط العملية بطريقة للحصول على أقصى عائد لـ CH 4. يظهر رسم تخطيطي مبسط لأهم التفاعلات التي تحدث في هذه العملية في الشكل. 1.7
الطاقة الشمسية هي أكبر مصدر للطاقة في العالم. إن انخفاض الطاقة الشمسية على 0.1٪ فقط من مساحة اليابسة في الولايات المتحدة يعادل كل الطاقة المستهلكة حاليًا في الولايات المتحدة. تكمن الصعوبة في استخدام الطاقة الشمسية في أنها مشتتة للغاية وغير متسقة في الوقت وتعتمد على الظروف الجوية. الأجهزة التي تحول الطاقة الشمسية إلى طاقة كهربائية حاليًا ليست فعالة بدرجة كافية. واحد من الطرق الممكنةاستخدام الطاقة الشمسية لإنشاء "مزارع الطاقة". يمكن لمثل هذه المزارع أن تزرع بسرعة محاصيل كبيرة من نباتات مختلفة ، ثم تحرق هذه النباتات للحصول على الطاقة. يمكن أن تكون الطاقة الشمسية حاليا بمثابة يساعدلتدفئة المساكن مع التقليدية ؛ يساعد استخدام سخانات المياه بالطاقة الشمسية والترتيب المدروس لجدران ونوافذ المنازل في خلق درجة الحرارة المطلوبة في المساكن والحفاظ عليها.
لاختتام المناقشة ، نلاحظ أن تركيزنا الأساسي كان على منع أزمة الطاقة من خلال خلق مصادر طاقة جديدة.
ومع ذلك ، يمكن التعامل مع حل هذه المشكلة من الجانب الآخر - عن طريق تقليل مستوى استهلاك الطاقة للفرد وتكاليف الطاقة غير المنتجة. ربما تكون هذه الطريقة في توفير الطاقة هي الطريقة الأكثر منطقية للخروج.
كرر المواد