خلية الوقودهو جهاز يولد بكفاءة تيارًا مباشرًا وحرارة من وقود غني بالهيدروجين عن طريق الكهرباء تفاعل كيميائي.
تشبه خلية الوقود البطارية في أنها تولد تيارًا مباشرًا من خلال تفاعل كيميائي. مرة أخرى ، مثل البطارية ، تشتمل خلية الوقود على أنود ، وكاثود ، وإلكتروليت. ومع ذلك ، على عكس البطاريات ، لا يمكن لخلايا الوقود تخزين الطاقة الكهربائية ولا تفريغها ولا تتطلب الكهرباء لإعادة شحنها. يمكن لخلايا الوقود أن تولد الكهرباء باستمرار طالما أنها مزودة بالوقود والهواء. المصطلح الصحيح لوصف خلية وقود عاملة هو نظام الخلية ، حيث يتطلب بعض الأنظمة المساعدة لتعمل بشكل صحيح.
على عكس مولدات الطاقة الأخرى مثل محركات الاحتراق الداخلي أو التوربينات التي تعمل بالغاز والفحم والزيت وما إلى ذلك ، فإن خلايا الوقود لا تحرق الوقود. هذا يعني عدم وجود دوارات صاخبة عالية الضغط ، ولا ضوضاء عادم عالية ، ولا اهتزازات. تولد خلايا الوقود الكهرباء من خلال تفاعل كهروكيميائي صامت. ميزة أخرى لخلايا الوقود هي أنها تحول الطاقة الكيميائية للوقود مباشرة إلى كهرباء وحرارة وماء.
تتميز خلايا الوقود بكفاءة عالية ولا تنتج كميات كبيرة من غازات الدفيئة مثل ثاني أكسيد الكربون والميثان وأكسيد النيتروز. الانبعاثات الوحيدة من تشغيل خلايا الوقود هي الماء على شكل بخار وكمية صغيرة من ثاني أكسيد الكربون ، والتي لا تنبعث على الإطلاق إذا تم استخدام الهيدروجين النقي كوقود. يتم تجميع خلايا الوقود في مجموعات ثم في وحدات وظيفية فردية.
مبدأ عمل خلايا الوقود
تولد خلايا الوقود الكهرباء والحرارة بسبب التفاعل الكهروكيميائي المستمر باستخدام إلكتروليت وكاثود وأنود.
يتم فصل القطب الموجب والكاثود بواسطة إلكتروليت يقوم بتوصيل البروتونات. بعد أن يدخل الهيدروجين في القطب الموجب ويدخل الأكسجين في الكاثود ، يبدأ تفاعل كيميائي ينتج عنه تيار كهربائي وحرارة وماء. على محفز الأنود ، ينفصل الهيدروجين الجزيئي ويفقد الإلكترونات. يتم توصيل أيونات الهيدروجين (البروتونات) عبر الإلكتروليت إلى القطب السالب ، بينما يتم تمرير الإلكترونات عبر الإلكتروليت وتمر عبر الجزء الخارجي دائرة كهربائية، مما يخلق تيارًا مباشرًا يمكن استخدامه لتشغيل المعدات. في محفز الكاثود ، يتحد جزيء الأكسجين مع الإلكترون (الذي يتم توفيره من الاتصالات الخارجية) والبروتون الوارد ، ويشكل الماء ، وهو منتج التفاعل الوحيد (في شكل بخار و / أو سائل).
يوجد أدناه رد الفعل المقابل:
تفاعل الأنود: 2H2 => 4H + 4e-
رد فعل عند الكاثود: O2 + 4H + 4e- => 2H2O
تفاعل العنصر العام: 2H2 + O2 => 2H2O
أنواع خلايا الوقود
على غرار وجود أنواع مختلفة من محركات الاحتراق الداخلي ، هناك أنواع مختلفة من خلايا الوقود - يعتمد اختيار النوع المناسب من خلايا الوقود على تطبيقه.تنقسم خلايا الوقود إلى درجة حرارة عالية ودرجة حرارة منخفضة. تتطلب خلايا الوقود ذات درجة الحرارة المنخفضة هيدروجينًا نقيًا نسبيًا كوقود.
هذا يعني غالبًا أن معالجة الوقود مطلوبة لتحويل الوقود الأساسي (مثل الغاز الطبيعي) إلى هيدروجين نقي. تستهلك هذه العملية طاقة إضافية وتتطلب معدات خاصة. لا تحتاج خلايا الوقود ذات درجة الحرارة المرتفعة إلى هذا الإجراء الإضافي ، حيث يمكنها "تحويل الوقود داخليًا" عند درجات حرارة مرتفعة ، مما يعني أنه لا توجد حاجة للاستثمار في البنية التحتية للهيدروجين.
عناصر الوقود على الكربونات المنصهرة (MCFC).
خلايا الوقود بالكهرباء المنصهرة عبارة عن خلايا وقود عالية الحرارة. تسمح درجة حرارة التشغيل العالية بالاستخدام المباشر للغاز الطبيعي بدون معالج وقود وغاز وقود منخفض الحرارة. القيمة الحراريةالوقود عمليات الانتاجومن مصادر أخرى. تم تطوير هذه العملية في منتصف الستينيات. منذ ذلك الوقت ، تم تحسين تكنولوجيا التصنيع والأداء والموثوقية.
يختلف تشغيل RCFC عن خلايا الوقود الأخرى. تستخدم هذه الخلايا إلكتروليت من خليط من أملاح الكربونات المنصهرة. حاليًا ، يتم استخدام نوعين من المخاليط: كربونات الليثيوم وكربونات البوتاسيوم أو كربونات الليثيوم وكربونات الصوديوم. لإذابة أملاح الكربونات وتحقيق درجة عالية من تنقل الأيونات في الإلكتروليت ، تعمل خلايا الوقود ذات المنحل بالكهرباء المنصهرة في درجات حرارة عالية (650 درجة مئوية). تتراوح الكفاءة بين 60-80٪.
عند تسخينها لدرجة حرارة 650 درجة مئوية ، تصبح الأملاح موصلًا لأيونات الكربونات (CO32-). تمر هذه الأيونات من القطب السالب إلى الأنود حيث تتحد مع الهيدروجين لتكوين الماء وثاني أكسيد الكربون والإلكترونات الحرة. يتم إرسال هذه الإلكترونات عبر دائرة كهربائية خارجية إلى الكاثود ، لتوليد التيار الكهربائي والحرارة كمنتج ثانوي.
تفاعل الأنود: CO32- + H2 => H2O + CO2 + 2e-
رد فعل عند الكاثود: CO2 + 1 / 2O2 + 2e- => CO32-
تفاعل العنصر العام: H2 (g) + 1 / 2O2 (g) + CO2 (cathode) => H2O (g) + CO2 (anode)
درجات حرارة التشغيل العالية لخلايا وقود الكربونات المنصهرة لها مزايا معينة. في درجات حرارة عالية ، يحدث الإصلاح الداخلي غاز طبيعي، مما يلغي الحاجة إلى معالج الوقود. بالإضافة إلى ذلك ، تشمل المزايا القدرة على استخدام مواد البناء القياسية ، مثل ألواح الفولاذ المقاوم للصدأ ومحفز النيكل على الأقطاب الكهربائية. يمكن استخدام الحرارة المهدرة لتوليد بخار عالي الضغط لمختلف التطبيقات الصناعية والتجارية.
درجات حرارة التفاعل العالية في المنحل بالكهرباء لها مزاياها أيضًا. يستغرق تطبيق درجات الحرارة المرتفعة وقتًا طويلاً للوصول إلى ظروف التشغيل المثلى ، ويتفاعل النظام بشكل أبطأ مع التغيرات في استهلاك الطاقة. تسمح هذه الخصائص باستخدام أنظمة خلايا الوقود مع إلكتروليت الكربونات المنصهر في ظروف طاقة ثابتة. تمنع درجات الحرارة المرتفعة تلف خلايا الوقود عن طريق أول أكسيد الكربون ، "التسمم" ، إلخ.
خلايا وقود الكربونات المنصهرة مناسبة للاستخدام على نطاق واسع منشآت ثابتة. يتم إنتاج محطات توليد الطاقة الحرارية التي تبلغ طاقتها الكهربائية 2.8 ميجاوات صناعيًا. يجري تطوير محطات بقدرة إنتاج تصل إلى 100 ميغاواط.
خلايا الوقود على أساس حمض الفوسفوريك (PFC).
كانت خلايا الوقود القائمة على حامض الفوسفوريك (orthophosphoric) هي خلايا الوقود الأولى للاستخدام التجاري. تم تطوير هذه العملية في منتصف الستينيات وتم اختبارها منذ السبعينيات. منذ ذلك الحين ، تم زيادة الاستقرار والأداء والتكلفة.
تستخدم خلايا الوقود القائمة على حمض الفوسفوريك (orthophosphoric) إلكتروليتًا يعتمد على حمض الفوسفوريك (H3PO4) بتركيز يصل إلى 100٪. تكون الموصلية الأيونية لحمض الفوسفوريك منخفضة في درجات الحرارة المنخفضة ، ولهذا السبب تستخدم خلايا الوقود هذه في درجات حرارة تصل إلى 150-220 درجة مئوية.
حامل الشحنة في خلايا الوقود من هذا النوع هو الهيدروجين (H + ، بروتون). تحدث عملية مماثلة في خلايا وقود غشاء تبادل البروتونات (MEFCs) ، حيث ينقسم الهيدروجين المزود إلى القطب الموجب إلى بروتونات وإلكترونات. تمر البروتونات عبر الإلكتروليت وتتحد مع الأكسجين من الهواء عند القطب السالب لتكوين الماء. يتم توجيه الإلكترونات على طول دائرة كهربائية خارجية ، ويتم توليد تيار كهربائي. فيما يلي التفاعلات التي تولد الكهرباء والحرارة.
تفاعل الأنود: 2H2 => 4H + 4e-
التفاعل عند الكاثود: O2 (g) + 4H + + 4e- => 2H2O
تفاعل العنصر العام: 2H2 + O2 => 2H2O
تزيد كفاءة خلايا الوقود المعتمدة على حامض الفوسفوريك (orthophosphoric) عن 40٪ عند توليد الطاقة الكهربائية. في الإنتاج المشترك للحرارة والكهرباء ، تبلغ الكفاءة الإجمالية حوالي 85٪. بالإضافة إلى ذلك ، نظرًا لدرجات حرارة التشغيل ، يمكن استخدام الحرارة المهدرة لتسخين المياه وتوليد البخار عند الضغط الجوي.
يعد الأداء العالي لمحطات الطاقة الحرارية على خلايا الوقود المعتمدة على حامض الفوسفوريك (orthophosphoric) في الإنتاج المشترك للحرارة والكهرباء أحد مزايا هذا النوع من خلايا الوقود. تستخدم المصانع أول أكسيد الكربون بتركيز حوالي 1.5٪ ، مما يوسع بشكل كبير من اختيار الوقود. بالإضافة إلى ذلك ، لا يؤثر ثاني أكسيد الكربون على المنحل بالكهرباء وتشغيل خلية الوقود ، ويعمل هذا النوع من الخلايا مع الوقود الطبيعي المعدل. البناء البسيط وتقلب الإلكتروليت المنخفض والاستقرار المتزايد هي أيضًا مزايا هذا النوع من خلايا الوقود.
يتم إنتاج محطات الطاقة الحرارية التي تنتج طاقة كهربائية تصل إلى 400 كيلوواط صناعيًا. اجتازت منشآت 11 ميغاواط الاختبارات ذات الصلة. يجري تطوير محطات بقدرة إنتاج تصل إلى 100 ميغاواط.
خلايا الوقود بغشاء التبادل البروتوني (PME)
تعتبر خلايا وقود غشاء التبادل البروتوني أفضل نوع من خلايا الوقود لتوليد طاقة السيارة ، والتي يمكن أن تحل محل البنزين و محركات الديزلالاحتراق الداخلي. تم استخدام خلايا الوقود هذه لأول مرة بواسطة وكالة ناسا لبرنامج الجوزاء. اليوم ، يتم تطوير وعرض التركيبات على MOPFC بقوة 1 واط إلى 2 كيلو واط.
تستخدم خلايا الوقود هذه غشاء بوليمر صلب (غشاء بلاستيكي رفيع) مثل المنحل بالكهرباء. عند تشريبه بالماء ، يمر هذا البوليمر بالبروتونات ، لكنه لا يوصل الإلكترونات.
الوقود هو الهيدروجين ، وحامل الشحنة هو أيون الهيدروجين (بروتون). عند الأنود ، يتم فصل جزيء الهيدروجين إلى أيون هيدروجين (بروتون) وإلكترونات. تمر أيونات الهيدروجين عبر الإلكتروليت إلى القطب السالب ، بينما تتحرك الإلكترونات حول الدائرة الخارجية وتنتج طاقة كهربائية. يتم تغذية الأكسجين ، المأخوذ من الهواء ، إلى الكاثود ويتحد مع الإلكترونات وأيونات الهيدروجين لتكوين الماء. تحدث التفاعلات التالية على الأقطاب الكهربائية:
تفاعل الأنود: 2H2 + 4OH- => 4H2O + 4e-
رد فعل عند الكاثود: O2 + 2H2O + 4e- => 4OH-
تفاعل العنصر العام: 2H2 + O2 => 2H2O
بالمقارنة مع الأنواع الأخرى من خلايا الوقود ، تنتج خلايا وقود غشاء تبادل البروتون مزيدًا من الطاقة لحجم أو وزن معين لخلية الوقود. تتيح هذه الميزة أن تكون مدمجة وخفيفة الوزن. بالإضافة إلى ذلك ، درجة حرارة التشغيل أقل من 100 درجة مئوية ، مما يسمح لك ببدء التشغيل بسرعة. هذه الخصائص ، بالإضافة إلى القدرة على تغيير خرج الطاقة بسرعة ، ليست سوى بعض الميزات التي تجعل خلايا الوقود هذه مرشحًا رئيسيًا للاستخدام في المركبات.
ميزة أخرى هي أن المنحل بالكهرباء مادة صلبة وليست سائلة. يكون الاحتفاظ بالغازات عند الكاثود والأنود أسهل مع وجود إلكتروليت صلب ، وبالتالي فإن إنتاج خلايا الوقود هذه أرخص. بالمقارنة مع الإلكتروليتات الأخرى ، فإن استخدام إلكتروليت صلب لا يسبب مشاكل مثل الاتجاه ، وهناك مشاكل أقل بسبب حدوث التآكل ، مما يؤدي إلى استدامة أطول للخلية ومكوناتها.
خلايا وقود الأكسيد الصلب (SOFC)
خلايا وقود الأكسيد الصلب هي خلايا الوقود ذات أعلى درجة حرارة تشغيل. يمكن أن تختلف درجة حرارة التشغيل من 600 درجة مئوية إلى 1000 درجة مئوية ، مما يسمح باستخدام أنواع مختلفة من الوقود دون معالجة مسبقة خاصة. للتعامل مع درجات الحرارة المرتفعة هذه ، يكون الإلكتروليت المستخدم عبارة عن أكسيد معدن صلب رقيق قائم على السيراميك ، وغالبًا ما يكون سبيكة من الإيتريوم والزركونيوم ، وهو موصل لأيونات الأكسجين (O2-). تتطور تقنية استخدام خلايا وقود الأكسيد الصلب منذ أواخر الخمسينيات. ولها تكوينان: مستو وأنبوبي.
يوفر المنحل بالكهرباء الصلب انتقالًا محكمًا للغاز من قطب كهربائي إلى آخر ، بينما توجد الإلكتروليتات السائلة في ركيزة مسامية. حامل الشحنة في خلايا الوقود من هذا النوع هو أيون الأكسجين (О2-). عند الكاثود ، يتم فصل جزيئات الأكسجين من الهواء إلى أيون أكسجين وأربعة إلكترونات. تمر أيونات الأكسجين عبر المنحل بالكهرباء وتتحد مع الهيدروجين لتكوين أربعة إلكترونات حرة. يتم توجيه الإلكترونات عبر دائرة كهربائية خارجية ، مما يؤدي إلى توليد تيار كهربائي وحرارة مهدرة.
تفاعل الأنود: 2H2 + 2O2- => 2H2O + 4e-
رد فعل عند الكاثود: O2 + 4e- => 2O2-
تفاعل العنصر العام: 2H2 + O2 => 2H2O
كفاءة الطاقة الكهربائية المتولدة هي الأعلى من بين جميع خلايا الوقود - حوالي 60٪. بالإضافة إلى ذلك ، تسمح درجات حرارة التشغيل المرتفعة بتوليد الحرارة والطاقة معًا لتوليد بخار عالي الضغط. يؤدي الجمع بين خلية وقود عالية الحرارة مع التوربينات إلى إنشاء خلية وقود هجينة لزيادة كفاءة توليد الطاقة الكهربائية بنسبة تصل إلى 70٪.
تعمل خلايا وقود الأكسيد الصلب في درجات حرارة عالية جدًا (600 درجة مئوية - 1000 درجة مئوية) ، مما يؤدي إلى وقت طويل للوصول إلى ظروف التشغيل المثلى ، ويكون النظام أبطأ في الاستجابة للتغيرات في استهلاك الطاقة. في درجات حرارة التشغيل المرتفعة هذه ، لا يلزم أي محول لاستعادة الهيدروجين من الوقود ، مما يسمح لمحطة الطاقة الحرارية بالعمل بوقود غير نقي نسبيًا من تغويز الفحم أو غازات النفايات ، وما شابه. أيضًا ، تعتبر خلية الوقود هذه ممتازة لتطبيقات الطاقة العالية ، بما في ذلك محطات الطاقة المركزية الصناعية والكبيرة. وحدات منتجة صناعياً بطاقة كهربائية ناتجة 100 كيلو وات.
خلايا الوقود مع أكسدة الميثانول المباشرة (DOMTE)
إن تقنية استخدام خلايا الوقود مع الأكسدة المباشرة للميثانول تمر بفترة من التطور النشط. لقد نجحت في ترسيخ مكانتها في مجال تشغيل الهواتف المحمولة وأجهزة الكمبيوتر المحمولة ، وكذلك لإنشاء مصادر طاقة محمولة. إلى ماذا يهدف التطبيق المستقبلي لهذه العناصر.
يشبه هيكل خلايا الوقود مع الأكسدة المباشرة للميثانول خلايا الوقود بغشاء تبادل البروتون (MOFEC) ، أي يستخدم البوليمر كإلكتروليت ، ويستخدم أيون الهيدروجين (بروتون) كحامل شحنة. ومع ذلك ، يتأكسد الميثانول السائل (CH3OH) في وجود الماء عند الأنود ، ويطلق ثاني أكسيد الكربون وأيونات الهيدروجين والإلكترونات ، والتي يتم توجيهها من خلال دائرة كهربائية خارجية ، ويتولد تيار كهربائي. تمر أيونات الهيدروجين عبر الإلكتروليت وتتفاعل مع الأكسجين من الهواء والإلكترونات من الدائرة الخارجية لتكوين الماء عند الأنود.
تفاعل الأنود: CH3OH + H2O => CO2 + 6H + + 6e-
التفاعل عند الكاثود: 3 / 2O2 + 6H + + 6e- => 3H2O
تفاعل العنصر العام: CH3OH + 3 / 2O2 => CO2 + 2H2O
بدأ تطوير خلايا الوقود هذه في أوائل التسعينيات. بعد تطوير المحفزات المحسنة ، وبفضل الابتكارات الحديثة الأخرى ، تمت زيادة كثافة الطاقة وكفاءتها بنسبة تصل إلى 40٪.
تم اختبار هذه العناصر في نطاق درجة حرارة 50-120 درجة مئوية. مع درجات حرارة التشغيل المنخفضة وعدم الحاجة إلى محول ، فإن خلايا وقود الميثانول المباشر هي أفضل مرشح للتطبيقات التي تتراوح من الهواتف المحمولة والمنتجات الاستهلاكية الأخرى إلى محركات السيارات. وميزة هذا النوع من خلايا الوقود هي صغر أبعادها ، نتيجة استخدام الوقود السائل ، وعدم الحاجة إلى استخدام المحول.
خلايا الوقود القلوية (AFC)
تعد خلايا الوقود القلوية (ALFCs) واحدة من أكثر التقنيات التي تمت دراستها وقد تم استخدامها منذ منتصف الستينيات. من قبل وكالة ناسا في برامج أبولو ومكوك الفضاء. على متن هذه المركبات الفضائية ، تنتج خلايا الوقود الكهرباء ومياه الشرب. تعد خلايا الوقود القلوية من أكثر الخلايا كفاءة في توليد الكهرباء ، حيث تصل كفاءة توليد الطاقة إلى 70٪.
تستخدم خلايا الوقود القلوية إلكتروليتًا ، أي محلول مائي من هيدروكسيد البوتاسيوم ، موجود في مصفوفة مسامية ومستقرة. قد يختلف تركيز هيدروكسيد البوتاسيوم اعتمادًا على درجة حرارة التشغيل لخلية الوقود ، والتي تتراوح من 65 درجة مئوية إلى 220 درجة مئوية. حامل الشحنة في SFC هو أيون هيدروكسيد (OH-) ينتقل من الكاثود إلى الأنود ، حيث يتفاعل مع الهيدروجين لإنتاج الماء والإلكترونات. يعود الماء الناتج عند الأنود إلى القطب السالب ، مرة أخرى يولد أيونات الهيدروكسيد هناك. نتيجة لهذه السلسلة من التفاعلات التي تحدث في خلية الوقود ، يتم إنتاج الكهرباء وكمنتج ثانوي ، يتم إنتاج الحرارة:
تفاعل الأنود: 2H2 + 4OH- => 4H2O + 4e-
رد فعل عند الكاثود: O2 + 2H2O + 4e- => 4OH-
رد الفعل العام للنظام: 2H2 + O2 => 2H2O
ميزة مركبات الكربون الكلورية فلورية هي أن خلايا الوقود هذه هي الأرخص في التصنيع ، لأن المحفز المطلوب على الأقطاب الكهربائية يمكن أن يكون أي مادة أرخص من تلك المستخدمة كمحفزات لخلايا الوقود الأخرى. بالإضافة إلى ذلك ، تعمل مركبات الكربون الهيدروكلورية فلورية في درجة حرارة منخفضة نسبيًا وهي من بين أكثر خلايا الوقود كفاءة - يمكن أن تساهم هذه الخصائص على التوالي في توليد طاقة أسرع وكفاءة عالية في استهلاك الوقود.
إحدى السمات المميزة لـ SFC هي حساسيتها العالية لثاني أكسيد الكربون ، والتي يمكن احتواؤها في الوقود أو الهواء. يتفاعل ثاني أكسيد الكربون مع المنحل بالكهرباء ويسمه بسرعة ويقلل بشكل كبير من كفاءة خلية الوقود. لذلك ، يقتصر استخدام مركبات الكربون الهيدروفلورية على الأماكن المغلقة مثل المركبات الفضائية وتحت الماء ، ويجب أن تعمل على الهيدروجين والأكسجين النقيين. علاوة على ذلك ، فإن جزيئات مثل CO و H2O و CH4 ، والتي تعتبر آمنة لخلايا الوقود الأخرى ، وحتى بالنسبة لبعضها وقودًا ، ضارة بـ SFC.
خلايا وقود البوليمر المنحل بالكهرباء (PETE)
في حالة خلايا وقود البوليمر بالكهرباء ، يتكون غشاء البوليمر من ألياف بوليمر ذات مناطق مائية حيث يتم توصيل أيونات الماء H2O + (بروتون ، أحمر) بجزيء الماء. تمثل جزيئات الماء مشكلة بسبب بطء التبادل الأيوني. لذلك ، يتطلب الأمر تركيزًا عاليًا من الماء في كل من الوقود وعلى أقطاب العادم ، مما يحد من درجة حرارة التشغيل إلى 100 درجة مئوية.
خلايا الوقود الحمضية الصلبة (SCFC)
في خلايا الوقود الحمضية الصلبة ، لا يحتوي المنحل بالكهرباء (CsHSO4) على الماء. وبالتالي فإن درجة حرارة التشغيل هي 100-300 درجة مئوية. يسمح دوران أنيون SO42-أوكسي للبروتونات (الحمراء) بالتحرك كما هو موضح في الشكل.
عادةً ما تكون خلية الوقود الحمضي الصلب عبارة عن شطيرة يتم فيها وضع طبقة رقيقة جدًا من مركب حمض صلب بين قطبين مضغوطين بإحكام لضمان اتصال جيد. عند تسخينه ، يتبخر المكون العضوي ، ويترك من خلال المسام في الأقطاب الكهربائية ، ويحتفظ بقدرة الاتصالات العديدة بين الوقود (أو الأكسجين في الطرف الآخر من الخلايا) ، والإلكتروليت والأقطاب الكهربائية.
| نوع خلية الوقود | درجة حرارة العمل | كفاءة توليد الطاقة | نوع الوقود | منطقة التطبيق |
|---|---|---|---|---|
| RKTE | 550-700 درجة مئوية | 50-70% | المنشآت المتوسطة والكبيرة | |
| FKTE | 100 - 220 درجة مئوية | 35-40% | هيدروجين نقي | المنشآت الكبيرة |
| MOPTE | 30-100 درجة مئوية | 35-50% | هيدروجين نقي | المنشآت الصغيرة |
| SOFC | 450-1000 درجة مئوية | 45-70% | معظم أنواع الوقود الهيدروكربوني | المنشآت الصغيرة والمتوسطة والكبيرة |
| بومت | 20-90 درجة مئوية | 20-30% | الميثانول | الوحدات المحمولة |
| SHTE | 50 - 200 درجة مئوية | 40-65% | هيدروجين نقي | أبحاث الفضاء |
| بيت | 30-100 درجة مئوية | 35-50% | هيدروجين نقي | المنشآت الصغيرة |
انضم إلينا على
خلية الوقودهو جهاز كهروكيميائي مشابه للخلية الجلفانية ، ولكنه يختلف عنها في أنه يتم تغذية المواد الخاصة بالتفاعل الكهروكيميائي فيه من الخارج - على عكس الكمية المحدودة من الطاقة المخزنة في خلية أو بطارية جلفانية.

أرز. واحد. بعض خلايا الوقود
تقوم خلايا الوقود بتحويل الطاقة الكيميائية للوقود إلى كهرباء ، متجاوزة عمليات الاحتراق غير الفعالة التي تحدث مع خسائر كبيرة. نتيجة لتفاعل كيميائي ، يقومون بتحويل الهيدروجين والأكسجين إلى كهرباء. نتيجة لهذه العملية ، يتكون الماء ويتم إطلاق كمية كبيرة من الحرارة. تشبه خلية الوقود إلى حد بعيد البطارية التي يمكن شحنها ثم استخدامها لتخزين الطاقة الكهربائية. مخترع خلية الوقود هو ويليام آر جروف ، الذي ابتكرها في عام 1839. في خلية الوقود هذه ، تم استخدام محلول حمض الكبريتيك كإلكتروليت ، وتم استخدام الهيدروجين كوقود ، والذي يتحد مع الأكسجين في وسط مؤكسد. حتى وقت قريب ، كانت خلايا الوقود تستخدم فقط في المختبرات وعلى المركبات الفضائية.
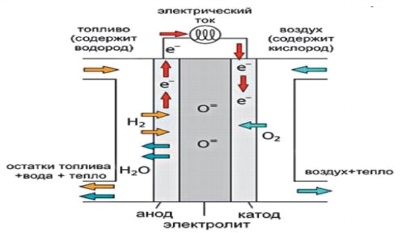
أرز. 2.
على عكس مولدات الطاقة الأخرى مثل محركات الاحتراق الداخلي أو التوربينات التي تعمل بالغاز والفحم والزيت وما إلى ذلك ، فإن خلايا الوقود لا تحرق الوقود. هذا يعني عدم وجود دوارات صاخبة عالية الضغط ، ولا ضوضاء عادم عالية ، ولا اهتزازات. تولد خلايا الوقود الكهرباء من خلال تفاعل كهروكيميائي صامت. ميزة أخرى لخلايا الوقود هي أنها تحول الطاقة الكيميائية للوقود مباشرة إلى كهرباء وحرارة وماء.
تتميز خلايا الوقود بكفاءة عالية ولا تنتج كميات كبيرة من غازات الدفيئة مثل ثاني أكسيد الكربون والميثان وأكسيد النيتروز. الانبعاثات الوحيدة من تشغيل خلايا الوقود هي الماء على شكل بخار وكمية صغيرة من ثاني أكسيد الكربون ، والتي لا تنبعث على الإطلاق إذا تم استخدام الهيدروجين النقي كوقود. يتم تجميع خلايا الوقود في مجموعات ثم في وحدات وظيفية فردية.
لا تحتوي خلايا الوقود على أجزاء متحركة (على الأقل ليس داخل الخلية نفسها) ، وبالتالي فهي لا تخضع لقانون كارنو. أي أنها ستتمتع بكفاءة تزيد عن 50٪ وتكون فعالة بشكل خاص في الأحمال المنخفضة. وبالتالي ، يمكن أن تكون المركبات التي تعمل بخلايا الوقود (وقد ثبت بالفعل أنها) أكثر كفاءة في استهلاك الوقود من المركبات التقليدية في ظروف القيادة الواقعية.
تولد خلية الوقود التيار الكهربائيجهد التيار المستمر ، والذي يمكن استخدامه لقيادة محرك كهربائي وتركيبات الإضاءة وغيرها الأنظمة الكهربائيةفي السيارة.
هناك عدة أنواع من خلايا الوقود تختلف في العمليات الكيميائية المستخدمة. عادة ما يتم تصنيف خلايا الوقود وفقًا لنوع الإلكتروليت الذي تستخدمه.
بعض أنواع خلايا الوقود واعدة للاستخدام كمحطات لتوليد الطاقة في محطات الطاقة ، في حين أن البعض الآخر مخصص للأجهزة المحمولة أو لقيادة السيارات.
1. خلايا الوقود القلوية (AFC)
خلية وقود قلوية- هذا هو أحد العناصر المطورة الأولى. تعد خلايا الوقود القلوية (ALFCs) واحدة من أكثر التقنيات التي خضعت للدراسة والمستخدمة منذ منتصف الستينيات من قبل وكالة ناسا في برامج أبولو ومكوك الفضاء. على متن هذه المركبات الفضائية ، تنتج خلايا الوقود الكهرباء ومياه الشرب.
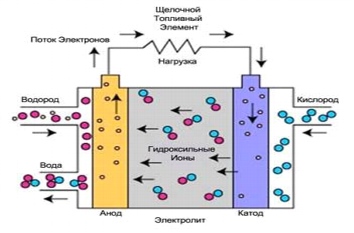
أرز. 3.
تعد خلايا الوقود القلوية من أكثر الخلايا كفاءة في توليد الكهرباء ، حيث تصل كفاءة توليد الطاقة إلى 70٪.
تستخدم خلايا الوقود القلوية إلكتروليتًا ، أي محلول مائي من هيدروكسيد البوتاسيوم ، موجود في مصفوفة مسامية ومستقرة. قد يختلف تركيز هيدروكسيد البوتاسيوم اعتمادًا على درجة حرارة التشغيل لخلية الوقود ، والتي تتراوح من 65 درجة مئوية إلى 220 درجة مئوية. حامل الشحنة في SFC هو أيون هيدروكسيد (OH-) ينتقل من الكاثود إلى الأنود ، حيث يتفاعل مع الهيدروجين لإنتاج الماء والإلكترونات. يعود الماء الناتج عند الأنود إلى القطب السالب ، مرة أخرى يولد أيونات الهيدروكسيد هناك. نتيجة لهذه السلسلة من التفاعلات التي تحدث في خلية الوقود ، يتم إنتاج الكهرباء وكمنتج ثانوي ، يتم إنتاج الحرارة:
تفاعل الأنود: 2H2 + 4OH- => 4H2O + 4e
رد فعل عند الكاثود: O2 + 2H2O + 4e- => 4OH
رد الفعل العام للنظام: 2H2 + O2 => 2H2O
ميزة مركبات الكربون الكلورية فلورية هي أن خلايا الوقود هذه هي الأرخص في التصنيع ، لأن المحفز المطلوب على الأقطاب الكهربائية يمكن أن يكون أي مادة أرخص من تلك المستخدمة كمحفزات لخلايا الوقود الأخرى. بالإضافة إلى ذلك ، تعمل مركبات الكربون الكلورية فلورية في درجات حرارة منخفضة نسبيًا وهي من بين أكثرها كفاءة.
إحدى السمات المميزة لـ SFC هي حساسيتها العالية لثاني أكسيد الكربون ، والتي يمكن احتواؤها في الوقود أو الهواء. يتفاعل ثاني أكسيد الكربون مع المنحل بالكهرباء ويسمه بسرعة ويقلل بشكل كبير من كفاءة خلية الوقود. لذلك ، يقتصر استخدام مركبات الكربون الكلورية فلورية على الأماكن المغلقة مثل المركبات الفضائية وتحت الماء ، فهي تعمل على الهيدروجين والأكسجين النقيين.
2. خلايا الوقود المصهور الكربوني (MCFC)
خلايا الوقود مع المنحل بالكهرباء المصهورهي خلايا وقود عالية الحرارة. تسمح درجة حرارة التشغيل المرتفعة بالاستخدام المباشر للغاز الطبيعي بدون معالج وقود وغاز وقود منخفض السعرات الحرارية من وقود العمليات ومصادر أخرى. تم تطوير هذه العملية في منتصف الستينيات. منذ ذلك الوقت ، تم تحسين تكنولوجيا التصنيع والأداء والموثوقية.
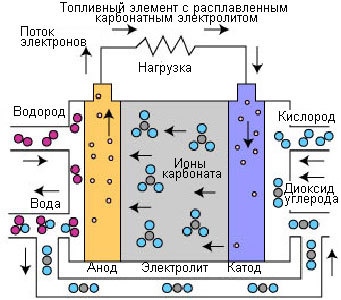
أرز. 4.
يختلف تشغيل RCFC عن خلايا الوقود الأخرى. تستخدم هذه الخلايا إلكتروليت من خليط من أملاح الكربونات المنصهرة. حاليًا ، يتم استخدام نوعين من المخاليط: كربونات الليثيوم وكربونات البوتاسيوم أو كربونات الليثيوم وكربونات الصوديوم. لإذابة أملاح الكربونات وتحقيق درجة عالية من تنقل الأيونات في الإلكتروليت ، تعمل خلايا الوقود ذات المنحل بالكهرباء المنصهرة في درجات حرارة عالية (650 درجة مئوية). تتراوح الكفاءة بين 60-80٪.
عند تسخينها لدرجة حرارة 650 درجة مئوية ، تصبح الأملاح موصلًا لأيونات الكربونات (CO32-). تنتقل هذه الأيونات من القطب السالب إلى القطب الموجب حيث تتحد مع الهيدروجين لتكوين الماء وثاني أكسيد الكربون والإلكترونات الحرة. يتم إرسال هذه الإلكترونات عبر دائرة كهربائية خارجية إلى الكاثود ، لتوليد التيار الكهربائي والحرارة كمنتج ثانوي.
تفاعل الأنود: CO32- + H2 => H2O + CO2 + 2e
رد فعل عند الكاثود: CO2 + 1 / 2O2 + 2e- => CO32-
تفاعل العنصر العام: H2 (g) + 1 / 2O2 (g) + CO2 (cathode) => H2O (g) + CO2 (anode)
درجات حرارة التشغيل العالية لخلايا وقود الكربونات المنصهرة لها مزايا معينة. الميزة هي القدرة على استخدام المواد القياسية (صفائح الفولاذ المقاوم للصدأ ومحفز النيكل على الأقطاب الكهربائية). يمكن استخدام الحرارة المهدرة لإنتاج بخار عالي الضغط. درجات حرارة التفاعل العالية في المنحل بالكهرباء لها مزاياها أيضًا. يستغرق استخدام درجات الحرارة المرتفعة وقتًا طويلاً للوصول إلى ظروف التشغيل المثلى ، ويتفاعل النظام بشكل أبطأ مع التغيرات في استهلاك الطاقة. تسمح هذه الخصائص باستخدام أنظمة خلايا الوقود مع إلكتروليت الكربونات المنصهر في ظروف طاقة ثابتة. درجات الحرارة المرتفعة تمنع تلف خلية الوقود عن طريق أول أكسيد الكربون ، "التسمم" ، إلخ.
خلايا وقود الكربونات المنصهرة مناسبة للاستخدام في المنشآت الثابتة الكبيرة. يتم إنتاج محطات توليد الطاقة الحرارية التي تبلغ طاقتها الكهربائية 2.8 ميجاوات صناعيًا. يجري تطوير محطات بقدرة إنتاج تصل إلى 100 ميغاواط.
3 - خلايا الوقود القائمة على حمض الفوسفوريك (PFC)
خلايا الوقود على أساس حمض الفوسفوريك (orthophosphoric)أصبحت خلايا الوقود الأولى للاستخدام التجاري. تم تطوير هذه العملية في منتصف الستينيات من القرن العشرين ، وتم إجراء الاختبارات منذ السبعينيات من القرن العشرين. نتيجة لذلك ، تم زيادة الاستقرار والأداء وخفضت التكلفة.
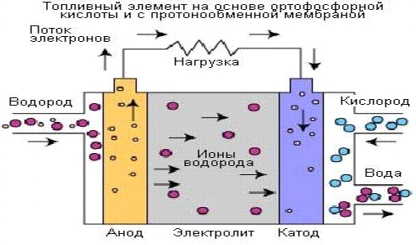
أرز. خمسة.
تستخدم خلايا الوقود القائمة على حمض الفوسفوريك (orthophosphoric) إلكتروليتًا يعتمد على حمض الفوسفوريك (H3PO4) بتركيز يصل إلى 100٪. الموصلية الأيونية لحمض الفوسفوريك منخفضة في درجات الحرارة المنخفضة ، لذلك يتم استخدام خلايا الوقود هذه في درجات حرارة تصل إلى 150-220 درجة مئوية.
حامل الشحنة في خلايا الوقود من هذا النوع هو الهيدروجين (H + ، بروتون). تحدث عملية مماثلة في خلايا وقود غشاء تبادل البروتونات (MEFCs) ، حيث ينقسم الهيدروجين المزود إلى القطب الموجب إلى بروتونات وإلكترونات. تمر البروتونات عبر الإلكتروليت وتتحد مع الأكسجين من الهواء عند القطب السالب لتكوين الماء. يتم توجيه الإلكترونات على طول دائرة كهربائية خارجية ، ويتم توليد تيار كهربائي. فيما يلي التفاعلات التي تولد الكهرباء والحرارة.
تفاعل الأنود: 2H2 => 4H + 4e
التفاعل عند الكاثود: O2 (g) + 4H + + 4e- => 2H2O
تفاعل العنصر العام: 2H2 + O2 => 2H2O
تزيد كفاءة خلايا الوقود المعتمدة على حامض الفوسفوريك (orthophosphoric) عن 40٪ عند توليد الطاقة الكهربائية. في الإنتاج المشترك للحرارة والكهرباء ، تبلغ الكفاءة الإجمالية حوالي 85٪. بالإضافة إلى ذلك ، نظرًا لدرجات حرارة التشغيل ، يمكن استخدام الحرارة المهدرة لتسخين المياه وتوليد البخار عند الضغط الجوي.
يعد الأداء العالي لمحطات الطاقة الحرارية على خلايا الوقود المعتمدة على حامض الفوسفوريك (orthophosphoric) في الإنتاج المشترك للحرارة والكهرباء أحد مزايا هذا النوع من خلايا الوقود. تستخدم المصانع أول أكسيد الكربون بتركيز حوالي 1.5٪ ، مما يوسع بشكل كبير من اختيار الوقود. البناء البسيط ، وانخفاض تقلب الإلكتروليت ، وزيادة الاستقرار هي أيضًا مزايا لخلايا الوقود هذه.
يتم إنتاج محطات الطاقة الحرارية التي تنتج طاقة كهربائية تصل إلى 400 كيلوواط صناعيًا. اجتازت المنشآت بسعة 11 ميغاواط الاختبارات ذات الصلة. يجري تطوير محطات بقدرة إنتاج تصل إلى 100 ميغاواط.
4. خلايا الوقود بغشاء تبادل البروتونات (MOFEC)
خلايا الوقود مع غشاء تبادل البروتونمن أفضل أنواع خلايا الوقود لتوليد طاقة المركبات ، والتي يمكن أن تحل محل محركات الاحتراق الداخلي للبنزين والديزل. تم استخدام خلايا الوقود هذه لأول مرة بواسطة وكالة ناسا لبرنامج الجوزاء. تم تطوير وعرض التركيبات على MOPFC بطاقة من 1 واط إلى 2 كيلو واط.
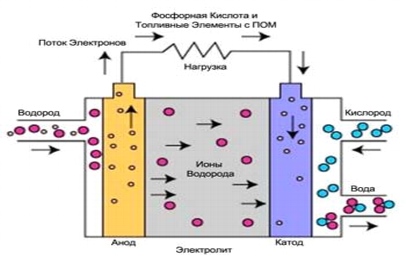
أرز. 6.
المنحل بالكهرباء في خلايا الوقود هذه عبارة عن غشاء بوليمر صلب (غشاء بلاستيكي رفيع). عند تشريبه بالماء ، يمر هذا البوليمر بالبروتونات ، لكنه لا يوصل الإلكترونات.
الوقود هو الهيدروجين ، وحامل الشحنة هو أيون الهيدروجين (بروتون). عند الأنود ، يتم فصل جزيء الهيدروجين إلى أيون هيدروجين (بروتون) وإلكترونات. تمر أيونات الهيدروجين عبر الإلكتروليت إلى القطب السالب ، بينما تتحرك الإلكترونات حول الدائرة الخارجية وتنتج طاقة كهربائية. يتم تغذية الأكسجين ، المأخوذ من الهواء ، إلى الكاثود ويتحد مع الإلكترونات وأيونات الهيدروجين لتكوين الماء. تحدث التفاعلات التالية عند الأقطاب الكهربائية: تفاعل الأنود: 2H2 + 4OH- => 4H2O + 4e تفاعل كاثود: O2 + 2H2O + 4e- => 4OH تفاعل الخلية الإجمالي: 2H2 + O2 => 2H2O مقارنة بأنواع أخرى من خلايا الوقود ، خلايا الوقود باستخدام غشاء تبادل البروتون ، ينتج المزيد من الطاقة لحجم أو وزن معين لخلية الوقود. تتيح هذه الميزة أن تكون مدمجة وخفيفة الوزن. بالإضافة إلى ذلك ، درجة حرارة التشغيل أقل من 100 درجة مئوية ، مما يسمح لك ببدء التشغيل بسرعة. هذه الخصائص ، بالإضافة إلى القدرة على تغيير ناتج الطاقة بسرعة ، ليست سوى بعض الميزات التي تجعل خلايا الوقود هذه مرشحًا رئيسيًا للاستخدام في المركبات.
ميزة أخرى هي أن الإلكتروليت مادة صلبة وليست سائلة. من الأسهل الاحتفاظ بالغازات عند الكاثود والأنود مع إلكتروليت صلب ، لذلك فإن تصنيع خلايا الوقود هذه أرخص في التصنيع. عند استخدام إلكتروليت صلب ، لا توجد صعوبات مثل التوجيه ، وقلة المشاكل بسبب حدوث التآكل ، مما يزيد من متانة الخلية ومكوناتها.
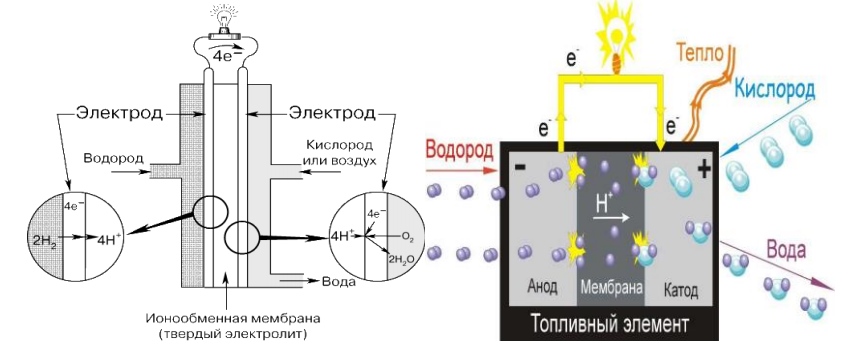
أرز. 7.
5. خلايا وقود الأكسيد الصلب (SOFC)
خلايا وقود الأكسيد الصلبهي خلايا الوقود ذات أعلى درجة حرارة تشغيل. يمكن أن تختلف درجة حرارة التشغيل من 600 درجة مئوية إلى 1000 درجة مئوية ، مما يسمح باستخدام أنواع مختلفة من الوقود دون معالجة مسبقة خاصة. للتعامل مع درجات الحرارة المرتفعة هذه ، يكون الإلكتروليت المستخدم عبارة عن أكسيد معدن صلب رقيق قائم على السيراميك ، وغالبًا ما يكون سبيكة من الإيتريوم والزركونيوم ، وهو موصل لأيونات الأكسجين (O2-). تتطور تقنية استخدام خلايا وقود الأكسيد الصلب منذ أواخر الخمسينيات من القرن الماضي ولها تكوينان: مستوٍ وأنبوبي.
يوفر المنحل بالكهرباء الصلب انتقالًا محكمًا للغاز من قطب كهربائي إلى آخر ، بينما توجد الإلكتروليتات السائلة في ركيزة مسامية. حامل الشحنة في خلايا الوقود من هذا النوع هو أيون الأكسجين (О2-). عند الكاثود ، يتم فصل جزيئات الأكسجين من الهواء إلى أيون أكسجين وأربعة إلكترونات. تمر أيونات الأكسجين عبر المنحل بالكهرباء وتتحد مع الهيدروجين لتكوين أربعة إلكترونات حرة. يتم توجيه الإلكترونات عبر دائرة كهربائية خارجية ، مما يؤدي إلى توليد تيار كهربائي وحرارة مهدرة.
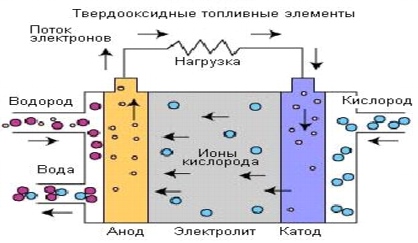
أرز. 8.
تفاعل الأنود: 2H2 + 2O2- => 2H2O + 4e
رد فعل عند الكاثود: O2 + 4e- => 2O2-
تفاعل العنصر العام: 2H2 + O2 => 2H2O
كفاءة إنتاج الطاقة الكهربائية هي الأعلى بين جميع خلايا الوقود - حوالي 60٪. بالإضافة إلى ذلك ، تسمح درجات حرارة التشغيل المرتفعة بتوليد الحرارة والطاقة معًا لتوليد بخار عالي الضغط. يؤدي الجمع بين خلية وقود عالية الحرارة مع التوربينات إلى إنشاء خلية وقود هجينة لزيادة كفاءة توليد الطاقة الكهربائية بنسبة تصل إلى 70٪.
تعمل خلايا وقود الأكسيد الصلب في درجات حرارة عالية جدًا (600 درجة مئوية إلى 1000 درجة مئوية) ، مما يؤدي إلى وقت طويل للوصول إلى ظروف التشغيل المثلى ، ويكون النظام أبطأ في الاستجابة للتغيرات في استهلاك الطاقة. في درجات حرارة التشغيل المرتفعة هذه ، لا يلزم أي محول لاستعادة الهيدروجين من الوقود ، مما يسمح لمحطة الطاقة الحرارية بالعمل بوقود غير نقي نسبيًا من تغويز الفحم أو غازات النفايات ، وما شابه. أيضًا ، تعتبر خلية الوقود هذه ممتازة لتطبيقات الطاقة العالية ، بما في ذلك محطات الطاقة المركزية الصناعية والكبيرة. وحدات منتجة صناعياً بطاقة كهربائية ناتجة 100 كيلو وات.
6. خلايا الوقود مع أكسدة الميثانول المباشرة (DOMTE)
خلايا الوقود مع أكسدة الميثانول المباشرةيتم استخدامها بنجاح في مجال تشغيل الهواتف المحمولة وأجهزة الكمبيوتر المحمولة ، وكذلك لإنشاء مصادر طاقة محمولة ، وهو ما يهدف إليه الاستخدام المستقبلي لهذه العناصر.
يشبه هيكل خلايا الوقود مع الأكسدة المباشرة للميثانول بنية خلايا الوقود بغشاء تبادل البروتون (MOFEC) ، أي يستخدم البوليمر كإلكتروليت ، ويستخدم أيون الهيدروجين (بروتون) كحامل شحنة. لكن الميثانول السائل (CH3OH) يتأكسد في وجود الماء عند الأنود ، ويطلق ثاني أكسيد الكربون وأيونات الهيدروجين والإلكترونات ، والتي يتم إرسالها عبر دائرة كهربائية خارجية ، ويتولد تيار كهربائي. تمر أيونات الهيدروجين عبر الإلكتروليت وتتفاعل مع الأكسجين من الهواء والإلكترونات من الدائرة الخارجية لتكوين الماء عند الأنود.
تفاعل الأنود: CH3OH + H2O => CO2 + 6H + + 6 e إلى 40٪.
تم اختبار هذه العناصر في نطاق درجة حرارة 50-120 درجة مئوية. نظرًا لانخفاض درجات حرارة التشغيل وعدم الحاجة إلى محول ، فإن خلايا الوقود هذه هي أفضل مرشح للتطبيقات في الهواتف المحمولة وغيرها من المنتجات الاستهلاكية ، وكذلك في محركات السيارات. ميزتها هي أيضا أبعاد صغيرة.
7. خلايا وقود البوليمر المنحل بالكهرباء (PETE)
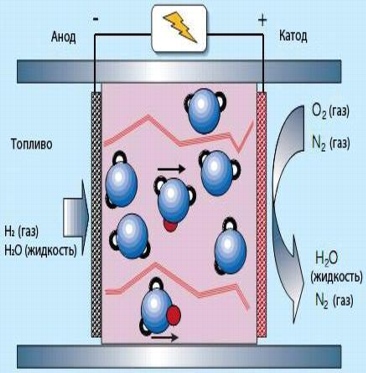
في حالة خلايا وقود البوليمر بالكهرباء ، يتكون غشاء البوليمر من ألياف بوليمر ذات مناطق مائية حيث يتم توصيل أيونات الماء H2O + (بروتون ، أحمر) بجزيء الماء. تمثل جزيئات الماء مشكلة بسبب بطء التبادل الأيوني. لذلك ، يتطلب الأمر تركيزًا عاليًا من الماء في كل من الوقود وعلى أقطاب العادم ، مما يحد من درجة حرارة التشغيل إلى 100 درجة مئوية.
8. خلايا الوقود الحمضية الصلبة (SCFC)
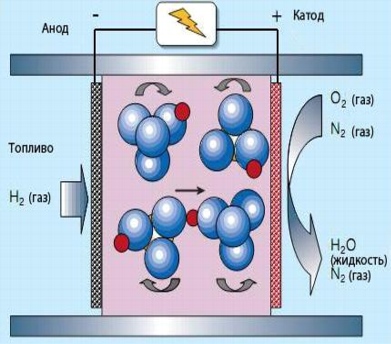
في خلايا الوقود الحمضية الصلبة ، لا يحتوي المنحل بالكهرباء (CsHSO4) على الماء. وبالتالي فإن درجة حرارة التشغيل هي 100-300 درجة مئوية. يسمح دوران SO42-oxyanions للبروتونات (الحمراء) بالتحرك كما هو موضح في الشكل. عادةً ما تكون خلية الوقود الحمضي الصلب عبارة عن شطيرة يتم فيها وضع طبقة رقيقة جدًا من مركب حمض صلب بين قطبين مضغوطين بإحكام لضمان اتصال جيد. عند تسخينه ، يتبخر المكون العضوي ، تاركًا من خلال المسام في الأقطاب الكهربائية ، محتفظًا بقدرة الاتصالات العديدة بين الوقود (أو الأكسجين في الطرف الآخر من الخلية) ، والإلكتروليت والأقطاب الكهربائية.
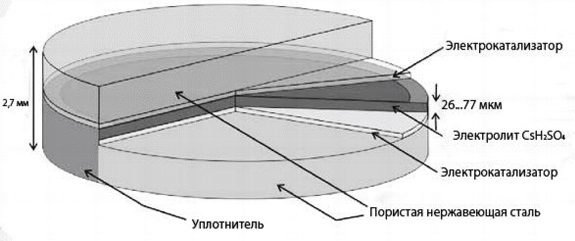
أرز. تسع.
9. مقارنة أهم خصائص خلايا الوقود
نوع خلية الوقود | درجة حرارة العمل | كفاءة توليد الطاقة | نوع الوقود | مجال |
المنشآت المتوسطة والكبيرة |
||||
هيدروجين نقي | المنشآت |
|||
هيدروجين نقي | المنشآت الصغيرة |
|||
معظم أنواع الوقود الهيدروكربوني | المنشآت الصغيرة والمتوسطة والكبيرة |
|||
محمول المنشآت |
||||
هيدروجين نقي | الفراغ استكشافها |
|||
هيدروجين نقي | المنشآت الصغيرة |
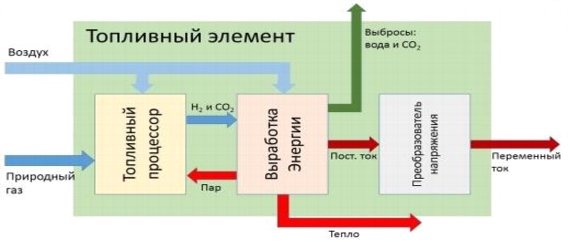
أرز. 10.
10. استخدام خلايا الوقود في السيارات
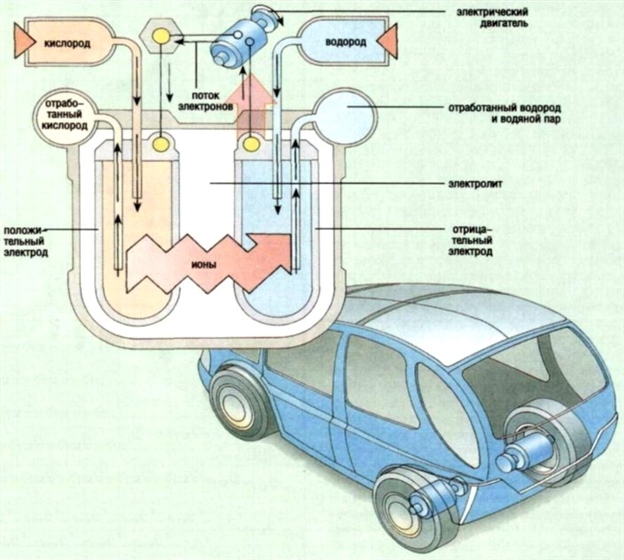
أرز. أحد عشر.
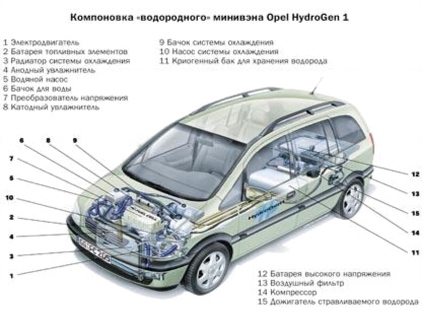
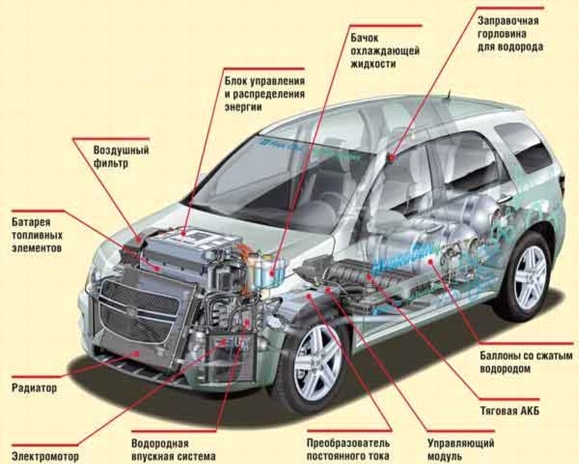
أرز. 12.
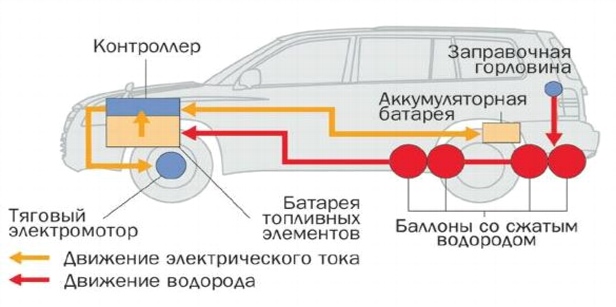
وصف:
تتناول هذه المقالة بمزيد من التفصيل هيكلها وتصنيفها ومزاياها وعيوبها ونطاقها وكفاءتها وتاريخ الإنشاء وآفاق الاستخدام الحديثة.
استخدام خلايا الوقود لتزويد المباني بالطاقة
الجزء 1
تتناول هذه المقالة بمزيد من التفصيل مبدأ تشغيل خلايا الوقود ، وتصميمها ، وتصنيفها ، ومزاياها وعيوبها ، ونطاقها ، وكفاءتها ، وتاريخ الإنشاء ، وآفاق الاستخدام الحديثة. في الجزء الثاني من المقال، الذي سيتم نشره في العدد القادم من مجلة ABOK ، يقدم أمثلة على المرافق التي تم فيها استخدام أنواع مختلفة من خلايا الوقود كمصادر للحرارة والكهرباء (أو للكهرباء فقط).
مقدمة
خلايا الوقود هي وسيلة فعالة للغاية وموثوقة ودائمة وصديقة للبيئة لتوليد الطاقة.
تستخدم خلايا الوقود في البداية فقط في صناعة الفضاء ، وتستخدم الآن بشكل متزايد في مجموعة متنوعة من المجالات - كمحطات طاقة ثابتة ، مصادر غير متصلة بالإنترنتإمداد التدفئة والطاقة للمباني ومحركات السيارات وإمدادات الطاقة لأجهزة الكمبيوتر المحمولة والهواتف المحمولة. بعض هذه الأجهزة عبارة عن نماذج أولية معملية ، وبعضها يخضع لاختبار ما قبل السلسلة أو يستخدم لأغراض توضيحية ، ولكن يتم إنتاج العديد من الطرز بكميات كبيرة واستخدامها في المشاريع التجارية.
مبدأ عمل خلايا الوقود
خلية الوقود (المولد الكهروكيميائي) هي جهاز يحول الطاقة الكيميائية للوقود (الهيدروجين) إلى طاقة كهربائية أثناء تفاعل كهروكيميائي بشكل مباشر ، على عكس التقنيات التقليدية التي تستخدم احتراق الوقود الصلب والسائل والغازي. يعتبر التحويل الكهروكيميائي المباشر للوقود فعالاً وجذاباً للغاية من وجهة النظر البيئية ، حيث يتم إطلاق الحد الأدنى من الملوثات أثناء التشغيل ، ولا توجد ضوضاء واهتزازات قوية.
من الناحية العملية ، تشبه خلية الوقود البطارية الجلفانية التقليدية. يكمن الاختلاف في حقيقة أن البطارية مشحونة في البداية ، أي مليئة "بالوقود". أثناء التشغيل ، يتم استهلاك "الوقود" وتفريغ البطارية. على عكس البطارية ، تستخدم خلية الوقود الوقود الذي يتم توفيره من مصدر خارجي لإنتاج الطاقة الكهربائية (الشكل 1).
لإنتاج الطاقة الكهربائية ، لا يمكن استخدام الهيدروجين النقي فحسب ، بل يمكن أيضًا استخدام المواد الخام الأخرى المحتوية على الهيدروجين ، مثل الغاز الطبيعي أو الأمونيا أو الميثانول أو البنزين. يستخدم الهواء العادي كمصدر للأكسجين ، وهو ضروري أيضًا للتفاعل.
عند استخدام الهيدروجين النقي كوقود ، فإن منتجات التفاعل ، بالإضافة إلى الطاقة الكهربائية ، هي الحرارة والماء (أو بخار الماء) ، أي لا تنبعث غازات في الغلاف الجوي تسبب تلوث الهواء أو تسبب تأثير الاحتباس الحراري. إذا تم استخدام مادة أولية تحتوي على الهيدروجين ، مثل الغاز الطبيعي ، كوقود ، فإن الغازات الأخرى ، مثل أكاسيد الكربون والنيتروجين ، ستكون منتجًا ثانويًا للتفاعل ، ولكن كميتها أقل بكثير مما كانت عليه عند حرق نفس الشيء كمية الغاز الطبيعي.
تسمى عملية التحويل الكيميائي للوقود من أجل إنتاج الهيدروجين الإصلاح ، والجهاز المقابل يسمى المصلح.
مزايا وعيوب خلايا الوقود
تعد خلايا الوقود أكثر كفاءة في استخدام الطاقة من محركات الاحتراق الداخلي لأنه لا توجد قيود ديناميكية حرارية على كفاءة الطاقة لخلايا الوقود. كفاءة خلايا الوقود 50٪ ، بينما كفاءة محركات الاحتراق الداخلي 12-15٪ ، وكفاءة محطات التوربينات البخارية لا تتعدى 40٪. باستخدام الحرارة والماء ، يتم زيادة كفاءة خلايا الوقود.
على عكس محركات الاحتراق الداخلي ، على سبيل المثال ، تظل كفاءة خلايا الوقود عالية جدًا حتى عندما لا تعمل بكامل طاقتها. بالإضافة إلى ذلك ، يمكن زيادة قوة خلايا الوقود ببساطة عن طريق إضافة كتل منفصلة ، بينما لا تتغير الكفاءة ، أي أن التركيبات الكبيرة فعالة مثل التركيبات الصغيرة. تسمح هذه الظروف باختيار مرن للغاية لتكوين المعدات وفقًا لرغبات العميل وتؤدي في النهاية إلى خفض تكاليف المعدات.
من المزايا المهمة لخلايا الوقود ملاءمتها للبيئة. انبعاثات الهواء من خلايا الوقود منخفضة جدًا لدرجة أنها في بعض مناطق الولايات المتحدة لا تتطلب تصاريح خاصة من وكالات جودة الهواء الحكومية.
يمكن وضع خلايا الوقود مباشرة في المبنى ، وبالتالي تقليل الخسائر أثناء نقل الطاقة ، ويمكن استخدام الحرارة الناتجة عن التفاعل لتزويد المبنى بالحرارة أو الماء الساخن. يمكن أن تكون المصادر المستقلة للحرارة وإمدادات الطاقة مفيدة للغاية في المناطق النائية وفي المناطق التي تتميز بنقص الكهرباء وارتفاع تكلفتها ، ولكن في نفس الوقت هناك احتياطيات من المواد الخام المحتوية على الهيدروجين (النفط والغاز الطبيعي) .
تتمثل مزايا خلايا الوقود أيضًا في توفر الوقود والموثوقية (لا توجد أجزاء متحركة في خلية الوقود) والمتانة وسهولة التشغيل.
تتمثل إحدى عيوب خلايا الوقود الرئيسية اليوم في تكلفتها المرتفعة نسبيًا ، ولكن يمكن التغلب على هذا القصور قريبًا - ينتج المزيد والمزيد من الشركات عينات تجارية من خلايا الوقود ، ويتم تحسينها باستمرار ، وتقل تكلفتها.
ومع ذلك ، فإن الاستخدام الأكثر كفاءة للهيدروجين النقي كوقود ، سيتطلب إنشاء بنية تحتية خاصة لتوليدها ونقلها. حاليًا ، تستخدم جميع التصاميم التجارية الغاز الطبيعي وأنواع الوقود المماثلة. يمكن للسيارات استخدام البنزين العادي ، مما سيسمح بالحفاظ على الشبكة الحالية المتطورة لمحطات الوقود. ومع ذلك ، فإن استخدام مثل هذا الوقود يؤدي إلى انبعاثات ضارة في الغلاف الجوي (وإن كانت منخفضة جدًا) ويعقد (وبالتالي يزيد من تكلفة) خلية الوقود. في المستقبل ، يتم النظر في إمكانية استخدام مصادر الطاقة المتجددة الصديقة للبيئة (على سبيل المثال ، الطاقة الشمسية أو طاقة الرياح) لتحليل الماء إلى هيدروجين وأكسجين عن طريق التحليل الكهربائي ، ثم تحويل الوقود الناتج في خلية وقود. يمكن أن تكون هذه المصانع المدمجة التي تعمل في دورة مغلقة مصدرًا للطاقة صديقًا للبيئة تمامًا وموثوقًا ودائمًا وفعالًا.
ميزة أخرى لخلايا الوقود هي أنها أكثر كفاءة عند استخدام كل من الطاقة الكهربائية والحرارية في نفس الوقت. ومع ذلك ، فإن إمكانية استخدام الطاقة الحرارية غير متوفرة في كل منشأة. في حالة استخدام خلايا الوقود لتوليد الطاقة الكهربائية فقط ، تنخفض كفاءتها بالرغم من أنها تفوق كفاءة التركيبات "التقليدية".
التاريخ والاستخدامات الحديثة لخلايا الوقود
تم اكتشاف مبدأ تشغيل خلايا الوقود في عام 1839. اكتشف العالم الإنجليزي ويليام روبرت جروف (1811-1896) أن عملية التحليل الكهربائي - تحلل الماء إلى هيدروجين وأكسجين بواسطة تيار كهربائي - يمكن عكسها ، أي يمكن دمج الهيدروجين والأكسجين في جزيئات الماء دون احتراق ، ولكن مع إطلاق الحرارة والتيار الكهربائي. أطلق جروف على الجهاز الذي تم فيه مثل هذا التفاعل "بطارية غاز" ، والتي كانت أول خلية وقود.
بدأ التطوير النشط لتقنيات خلايا الوقود بعد الحرب العالمية الثانية ، وهو مرتبط بصناعة الطيران. في ذلك الوقت ، أجريت عمليات بحث عن مصدر طاقة فعال وموثوق ، ولكن في نفس الوقت مضغوط تمامًا. في الستينيات ، اختار متخصصو وكالة ناسا (الإدارة الوطنية للملاحة الجوية والفضاء ، ناسا) خلايا الوقود كمصدر للطاقة للمركبات الفضائية لأبولو (الرحلات المأهولة إلى القمر) ، أبولو سويوز ، جيميني وبرامج سكايلاب. استخدمت أبولو ثلاث وحدات بقدرة 1.5 كيلو وات (2.2 كيلو وات ذروة الطاقة) باستخدام الهيدروجين والأكسجين المبردين لإنتاج الكهرباء والحرارة والماء. كانت كتلة كل تركيب 113 كجم. تعمل هذه الخلايا الثلاث بشكل متوازٍ ، لكن الطاقة التي تولدها وحدة واحدة كانت كافية لعودة آمنة. خلال 18 رحلة ، تراكمت خلايا الوقود ما مجموعه 10000 ساعة دون أي أعطال. حاليًا ، تُستخدم خلايا الوقود في مكوك الفضاء "مكوك الفضاء" ، والذي يستخدم ثلاث وحدات بقوة 12 واط ، والتي تولد كل الطاقة الكهربائية على متن المركبة الفضائية (الشكل 2). يتم استخدام المياه التي يتم الحصول عليها نتيجة تفاعل كهروكيميائي كمياه شرب ، وكذلك لمعدات التبريد.
في بلدنا ، كان العمل جاريًا أيضًا لإنشاء خلايا وقود لاستخدامها في الملاحة الفضائية. على سبيل المثال ، تم استخدام خلايا الوقود لتشغيل مكوك الفضاء السوفيتي بوران.
بدأ تطوير طرق للاستخدام التجاري لخلايا الوقود في منتصف الستينيات. تم تمويل هذه التطورات جزئياً من قبل المؤسسات الحكومية.
في الوقت الحالي ، يسير تطوير تقنيات استخدام خلايا الوقود في عدة اتجاهات. هذا هو إنشاء محطات طاقة ثابتة على خلايا الوقود (لكل من إمدادات الطاقة المركزية واللامركزية) ، ومحطات توليد الطاقة للمركبات (تم إنشاء عينات من السيارات والحافلات على خلايا الوقود ، بما في ذلك في بلدنا) (الشكل 3) ، و أيضًا مزودات الطاقة لمختلف الأجهزة المحمولة (أجهزة الكمبيوتر المحمولة ، والهواتف المحمولة ، وما إلى ذلك) (الشكل 4).
ويرد في الجدول أمثلة على استخدام خلايا الوقود في مختلف المجالات. واحد.
أحد النماذج التجارية الأولى لخلايا الوقود المصممة لتزويد المباني بالحرارة والطاقة المستقلة كان طراز PC25 A المصنوع من قبل ONSI Corporation (الآن United Technologies، Inc.). تنتمي خلية الوقود هذه بقوة اسمية تبلغ 200 كيلو وات إلى نوع الخلايا التي تحتوي على إلكتروليت يعتمد على حمض الفوسفوريك (خلايا وقود حمض الفوسفوريك ، PAFC). الرقم "25" في اسم النموذج يعني الرقم التسلسلي للتصميم. كانت معظم النماذج السابقة عبارة عن قطع تجريبية أو اختبارية ، مثل طراز "PC11" الذي يبلغ 12.5 كيلو وات والذي ظهر في السبعينيات. زادت النماذج الجديدة من الطاقة المأخوذة من خلية وقود واحدة ، كما خفضت التكلفة لكل كيلوواط من الطاقة المنتجة. حاليًا ، أحد أكثر النماذج التجارية كفاءة هو خلية الوقود PC25 Model C. مثل الطراز "A" ، هذه خلية وقود أوتوماتيكية بالكامل من نوع PAFC بقدرة 200 كيلو وات مصممة للتركيب مباشرة على الجسم الذي تتم خدمته كمصدر مستقل للحرارة والكهرباء. يمكن تركيب خلية الوقود هذه خارج المبنى. ظاهريًا ، يبلغ طوله 5.5 مترًا وعرضه 3 مترًا وارتفاعه 3 مترًا ويزن 18140 كجم. يتمثل الاختلاف عن النماذج السابقة في مُصلِح مُحسَّن وكثافة تيار أعلى.
| الجدول 1 نطاق خلايا الوقود |
|||||||||||||||
|
في بعض أنواع خلايا الوقود ، يمكن عكس العملية الكيميائية: من خلال تطبيق فرق جهد على الأقطاب الكهربائية ، يمكن أن يتحلل الماء إلى هيدروجين وأكسجين ، يتم تجميعهما على أقطاب كهربائية مسامية. عندما يتم توصيل الحمل ، ستبدأ خلية الوقود المتجدد هذه في توليد طاقة كهربائية.
يتمثل الاتجاه الواعد لاستخدام خلايا الوقود في استخدامها مع مصادر الطاقة المتجددة ، مثل الألواح الكهروضوئية أو توربينات الرياح. تتيح لك هذه التقنية تجنب تلوث الهواء تمامًا. تم التخطيط لإنشاء نظام مماثل ، على سبيل المثال ، في مركز تدريب آدم جوزيف لويس في أوبرلين (انظر ABOK ، 2002 ، رقم 5 ، ص 10). حاليًا ، تُستخدم الألواح الشمسية كأحد مصادر الطاقة في هذا المبنى. بالتعاون مع متخصصي وكالة ناسا ، تم تطوير مشروع لاستخدام الألواح الكهروضوئية لإنتاج الهيدروجين والأكسجين من الماء عن طريق التحليل الكهربائي. ثم يتم استخدام الهيدروجين في خلايا الوقود لتوليد الطاقة الكهربائية و ماء ساخن. سيسمح ذلك للمبنى بالحفاظ على أداء جميع الأنظمة خلال الأيام الملبدة بالغيوم وفي الليل.
مبدأ عمل خلايا الوقود
دعونا ننظر في مبدأ تشغيل خلية الوقود باستخدام أبسط عنصر مع غشاء تبادل البروتون (غشاء تبادل البروتون ، PEM) كمثال. يتكون هذا العنصر من غشاء بوليمر يوضع بين القطب الموجب (القطب الموجب) والكاثود (القطب السالب) مع محفزات الأنود والكاثود. يستخدم غشاء البوليمر كإلكتروليت. يظهر الرسم التخطيطي لعنصر PEM في الشكل. خمسة.
غشاء تبادل البروتون (PEM) عبارة عن مركب عضوي صلب رفيع (حوالي 2-7 ورقة سميكة من الورق العادي). يعمل هذا الغشاء كإلكتروليت: فهو يفصل المادة إلى أيونات موجبة وسالبة الشحنة في وجود الماء.
تحدث عملية الأكسدة عند القطب الموجب ، وتحدث عملية الاختزال عند القطب السالب. يتكون الأنود والكاثود في خلية PEM من مادة مسامية ، وهي مزيج من جزيئات الكربون والبلاتين. يعمل البلاتين كمحفز يعزز تفاعل التفكك. يصنع القطب الموجب والكاثود مساميًا للمرور الحر للهيدروجين والأكسجين عبرهما ، على التوالي.
يتم وضع القطب الموجب والكاثود بين لوحين معدنيين ، يزودان الهيدروجين والأكسجين بالقطب الموجب والكاثود ، ويزيلان الحرارة والماء ، وكذلك الطاقة الكهربائية.
تمر جزيئات الهيدروجين عبر القنوات الموجودة في اللوحة إلى القطب الموجب ، حيث تتحلل الجزيئات إلى ذرات فردية (الشكل 6).
الشكل 5 () رسم تخطيطي لخلية وقود غشاء تبادل البروتون (PEM) |
|
الشكل 6 () تدخل جزيئات الهيدروجين عبر القنوات الموجودة في اللوحة إلى القطب الموجب ، حيث تتحلل الجزيئات إلى ذرات فردية |
|
الشكل 7 () نتيجة الامتصاص الكيميائي في وجود محفز ، يتم تحويل ذرات الهيدروجين إلى بروتونات |
|
الشكل 8 () تنتشر أيونات الهيدروجين موجبة الشحنة عبر الغشاء إلى الكاثود ، ويتم توجيه تدفق الإلكترون إلى الكاثود من خلال دائرة كهربائية خارجية يتصل بها الحمل. |
|
الشكل 9 () يدخل الأكسجين المزود للكاثود ، في وجود محفز ، في تفاعل كيميائي مع أيونات الهيدروجين من غشاء تبادل البروتون والإلكترونات من الدائرة الكهربائية الخارجية. يتكون الماء نتيجة تفاعل كيميائي |
بعد ذلك ، نتيجة الامتصاص الكيميائي في وجود محفز ، يتم تحويل ذرات الهيدروجين ، التي تتبرع كل منها بإلكترون واحد ، إلى أيونات هيدروجين موجبة الشحنة H + ، أي البروتونات (الشكل 7).
تنتشر أيونات الهيدروجين موجبة الشحنة (البروتونات) عبر الغشاء إلى الكاثود ، ويتم توجيه تدفق الإلكترون إلى الكاثود من خلال دائرة كهربائية خارجية يتصل بها الحمل (مستهلك الطاقة الكهربائية) (الشكل 8).
يدخل الأكسجين المزود للكاثود ، في وجود محفز ، في تفاعل كيميائي مع أيونات الهيدروجين (البروتونات) من غشاء تبادل البروتون والإلكترونات من الدائرة الكهربائية الخارجية (الشكل 9). نتيجة لتفاعل كيميائي ، يتكون الماء.
التفاعل الكيميائي في خلية وقود من أنواع أخرى (على سبيل المثال ، مع إلكتروليت حمضي ، وهو محلول من حمض الفوسفوريك H 3 PO 4) مطابق تمامًا للتفاعل الكيميائي في خلية وقود مع غشاء تبادل بروتون.
في أي خلية وقود ، يتم إطلاق جزء من طاقة تفاعل كيميائي كحرارة.
إن تدفق الإلكترونات في الدائرة الخارجية هو تيار مباشر يستخدم لأداء العمل. يؤدي فتح الدائرة الخارجية أو إيقاف حركة أيونات الهيدروجين إلى إيقاف التفاعل الكيميائي.
تعتمد كمية الطاقة الكهربائية التي تنتجها خلية الوقود على نوع خلية الوقود والأبعاد الهندسية ودرجة الحرارة وضغط الغاز. توفر خلية وقود واحدة EMF أقل من 1.16 فولت. ومن الممكن زيادة حجم خلايا الوقود ، ولكن في الممارسة العملية ، يتم استخدام عدة خلايا متصلة بالبطاريات (الشكل 10).
جهاز خلية الوقود
لنفكر في جهاز خلية الوقود على مثال طراز PC25 Model C. يظهر مخطط خلية الوقود في الشكل. أحد عشر.
تتكون خلية الوقود "PC25 Model C" من ثلاثة أجزاء رئيسية: معالج الوقود وقسم توليد الطاقة الفعلي ومحول الجهد.
الجزء الرئيسي من خلية الوقود - قسم توليد الطاقة - عبارة عن كومة تتكون من 256 خلية وقود فردية. تشتمل تركيبة أقطاب خلايا الوقود على محفز بلاتيني. من خلال هذه الخلايا ، يتم توليد تيار كهربائي مباشر يبلغ 1400 أمبير بجهد 155 فولت. تبلغ أبعاد البطارية حوالي 2.9 م في الطول و 0.9 م في العرض والارتفاع.
نظرًا لأن العملية الكهروكيميائية تحدث عند درجة حرارة 177 درجة مئوية ، فمن الضروري تسخين البطارية في وقت بدء التشغيل وإزالة الحرارة منها أثناء التشغيل. للقيام بذلك ، تشتمل خلية الوقود على دائرة مياه منفصلة ، والبطارية مزودة بألواح تبريد خاصة.
يسمح لك معالج الوقود بتحويل الغاز الطبيعي إلى هيدروجين ، وهو أمر ضروري للتفاعل الكهروكيميائي. هذه العملية تسمى الإصلاح. العنصر الرئيسي لمعالج الوقود هو المصلح. في المصلح ، يتفاعل الغاز الطبيعي (أو أي وقود آخر يحتوي على الهيدروجين) مع البخار عند درجة حرارة عالية (900 درجة مئوية) وضغط مرتفع في وجود محفز نيكل. تحدث التفاعلات الكيميائية التالية:
CH 4 (ميثان) + H 2 O 3H 2 + CO
(ماص للحرارة التفاعل ، مع امتصاص الحرارة) ؛
ثاني أكسيد الكربون + H 2 O H 2 + CO 2
(يكون التفاعل طاردًا للحرارة ، مع إطلاق حرارة).
يتم التعبير عن رد الفعل الكلي بالمعادلة:
CH 4 (ميثان) + 2H 2 O 4H 2 + CO 2
(ماص للحرارة التفاعل ، مع امتصاص الحرارة).
لتوفير درجة الحرارة العالية المطلوبة لتحويل الغاز الطبيعي ، يتم إرسال جزء من الوقود المستهلك من مكدس خلايا الوقود إلى الموقد الذي يحافظ على وحدة الإصلاح عند درجة الحرارة المطلوبة.
يتم توليد البخار المطلوب لإعادة التشكيل من المكثفات المتكونة أثناء تشغيل خلية الوقود. في هذه الحالة ، يتم استخدام الحرارة المنبعثة من مكدس خلايا الوقود (الشكل 12).
يولد كومة خلايا الوقود تيارًا مباشرًا متقطعًا ، يتميز بجهد منخفض وتيار مرتفع. يستخدم محول الجهد لتحويله إلى تيار متردد صناعي قياسي. بالإضافة إلى ذلك ، تشتمل وحدة محول الجهد على العديد من أجهزة التحكم ودوائر قفل الأمان التي تسمح بإيقاف تشغيل خلية الوقود في حالة حدوث أعطال مختلفة.
في خلية الوقود هذه ، يمكن تحويل ما يقرب من 40٪ من الطاقة الموجودة في الوقود إلى طاقة كهربائية. تقريبًا نفس الشيء ، يمكن تحويل حوالي 40٪ من طاقة الوقود إلى طاقة حرارية، والذي يستخدم بعد ذلك كمصدر حرارة للتدفئة وإمدادات المياه الساخنة ولأغراض مماثلة. وبالتالي ، يمكن أن تصل الكفاءة الإجمالية لمثل هذا المصنع إلى 80٪.
من المزايا المهمة لمثل هذا المصدر للحرارة والكهرباء إمكانية وجوده عملية تلقائية. للصيانة ، لا يحتاج مالكو المنشأة التي تم تركيب خلية الوقود عليها إلى صيانة موظفين مدربين تدريباً خاصاً - يمكن إجراء الصيانة الدورية بواسطة موظفي المؤسسة المشغلة.
أنواع خلايا الوقود
حاليًا ، تُعرف عدة أنواع من خلايا الوقود ، والتي تختلف في تكوين الإلكتروليت المستخدم. الأنواع الأربعة التالية هي الأكثر انتشارًا (الجدول 2):
1. خلايا الوقود مع غشاء تبادل البروتون (خلايا وقود غشاء التبادل البروتوني ، PEMFC).
2. خلايا الوقود على أساس حامض الفوسفوريك (خلايا وقود حمض الفوسفوريك ، PAFC).
3. خلايا الوقود القائمة على الكربونات المنصهرة (خلايا وقود الكربونات المنصهرة ، MCFC).
4. خلايا وقود الأكسيد الصلب (خلايا وقود الأكسيد الصلب ، SOFC). حاليًا ، تم بناء أكبر أسطول من خلايا الوقود على أساس تقنية PAFC.
درجة حرارة التشغيل هي إحدى الخصائص الرئيسية للأنواع المختلفة من خلايا الوقود. من نواح كثيرة ، فإن درجة الحرارة هي التي تحدد نطاق خلايا الوقود. على سبيل المثال ، تعتبر درجات الحرارة المرتفعة أمرًا بالغ الأهمية لأجهزة الكمبيوتر المحمولة ، لذلك يتم تطوير خلايا وقود غشاء تبادل البروتونات ذات درجات حرارة تشغيل منخفضة لهذا الجزء من السوق.
بالنسبة لتزويد المباني بالطاقة المستقلة ، يلزم وجود خلايا وقود ذات سعة مركبة عالية ، وفي الوقت نفسه ، من الممكن استخدام الطاقة الحرارية ، وبالتالي ، يمكن أيضًا استخدام خلايا الوقود من أنواع أخرى لهذه الأغراض.
خلايا وقود غشاء التبادل البروتوني (PEMFC)
تعمل خلايا الوقود هذه في درجات حرارة تشغيل منخفضة نسبيًا (60-160 درجة مئوية). تتميز بكثافة طاقة عالية ، وتسمح لك بضبط طاقة الإخراج بسرعة ، ويمكن تشغيلها بسرعة. عيب هذا النوع من العناصر هو المتطلبات العالية لجودة الوقود ، لأن الوقود الملوث يمكن أن يتلف الغشاء. الطاقة الاسمية لخلايا الوقود من هذا النوع هي 1-100 كيلو واط.
تم تطوير خلايا وقود غشاء التبادل البروتوني في الأصل بواسطة شركة جنرال إلكتريك في الستينيات لصالح وكالة ناسا. يستخدم هذا النوع من خلايا الوقود مادة إلكتروليت بوليمرية صلبة تسمى غشاء تبادل البروتون (PEM). يمكن أن تتحرك البروتونات عبر غشاء تبادل البروتون ، لكن لا يمكن للإلكترونات المرور خلالها ، مما يؤدي إلى فرق جهد بين القطب السالب والأنود. نظرًا لبساطتها وموثوقيتها ، تم استخدام خلايا الوقود هذه كمصدر للطاقة على مركبة الفضاء المأهولة الجوزاء.
يستخدم هذا النوع من خلايا الوقود كمصدر للطاقة لمجموعة متنوعة من الأجهزة ، بما في ذلك النماذج الأولية والنماذج الأولية ، من الهواتف المحمولة إلى الحافلات وأنظمة الطاقة الثابتة. تسمح درجة حرارة التشغيل المنخفضة باستخدام هذه الخلايا لتشغيل أنواع مختلفة من الأجهزة الإلكترونية المعقدة. أقل كفاءة هو استخدامها كمصدر للحرارة وإمدادات الطاقة للمباني العامة والصناعية ، حيث تتطلب كميات كبيرة من الطاقة الحرارية. في الوقت نفسه ، تعد هذه العناصر واعدة كمصدر مستقل لإمداد الطاقة للمباني السكنية الصغيرة مثل الأكواخ المبنية في مناطق ذات مناخ حار.
| الجدول 2 أنواع خلايا الوقود |
||||||||||||||||||||
|
خلايا وقود حامض الفوسفوريك (PAFC)
تم بالفعل إجراء اختبارات خلايا الوقود من هذا النوع في أوائل السبعينيات. نطاق درجة حرارة التشغيل - 150-200 درجة مئوية. المجال الرئيسي للتطبيق هو المصادر المستقلة للحرارة وإمدادات الطاقة ذات الطاقة المتوسطة (حوالي 200 كيلو واط).
المنحل بالكهرباء المستخدم في خلايا الوقود هذه هو محلول حمض الفوسفوريك. الأقطاب الكهربائية مصنوعة من الورق المطلي بالكربون ، حيث يتم تشتيت محفز البلاتين.
تبلغ الكفاءة الكهربائية لخلايا وقود PAFC 37-42٪. ومع ذلك ، نظرًا لأن خلايا الوقود هذه تعمل عند درجة حرارة عالية بدرجة كافية ، فمن الممكن استخدام البخار المتولد نتيجة للتشغيل. في هذه الحالة ، يمكن أن تصل الكفاءة الإجمالية إلى 80٪.
لتوليد الطاقة ، يجب تحويل المادة الأولية المحتوية على الهيدروجين إلى هيدروجين نقي من خلال عملية إعادة التشكيل. على سبيل المثال ، إذا تم استخدام البنزين كوقود ، فيجب إزالة مركبات الكبريت ، حيث يمكن للكبريت إتلاف محفز البلاتين.
كانت خلايا الوقود PAFC هي أول خلايا وقود تجارية لها ما يبررها اقتصاديًا. كان النموذج الأكثر شيوعًا هو خلية الوقود PC25 بقدرة 200 كيلو وات التي تصنعها شركة ONSI (الآن United Technologies، Inc.) (الشكل 13). على سبيل المثال ، تُستخدم هذه العناصر كمصدر للحرارة والكهرباء في مركز للشرطة في سنترال بارك بنيويورك أو كمصدر إضافي للطاقة لمبنى كوندي ناست وفور تايمز سكوير. أكثر منصة كبيرةمن هذا النوع يتم اختباره كمحطة طاقة 11 ميجاوات في اليابان.
تستخدم خلايا الوقود التي تعتمد على حمض الفوسفوريك أيضًا كمصدر للطاقة في المركبات. على سبيل المثال ، في عام 1994 ، قامت H-Power Corp. وجامعة جورج تاون ووزارة الطاقة الأمريكية بتجهيز حافلة بمحطة طاقة 50 كيلو وات.
خلايا وقود الكربونات المنصهرة (MCFC)
تعمل خلايا الوقود من هذا النوع في درجات حرارة عالية جدًا - 600-700 درجة مئوية. تسمح درجات حرارة التشغيل هذه باستخدام الوقود مباشرة في الخلية نفسها ، دون الحاجة إلى مصلح منفصل. هذه العملية تسمى "الإصلاح الداخلي". إنه يسمح بتبسيط تصميم خلية الوقود بشكل كبير.
تتطلب خلايا الوقود القائمة على الكربونات المنصهرة وقتًا كبيرًا لبدء التشغيل ولا تسمح بضبط طاقة الخرج بسرعة ، لذا فإن مجال تطبيقها الرئيسي هو مصادر ثابتة كبيرة للحرارة والكهرباء. ومع ذلك ، فهي تتميز بكفاءة عالية في تحويل الوقود - 60٪ كفاءة كهربائية وما يصل إلى 85٪ كفاءة إجمالية.
في هذا النوع من خلايا الوقود ، يتكون المحلول الكهربائي من كربونات البوتاسيوم وأملاح كربونات الليثيوم التي يتم تسخينها إلى حوالي 650 درجة مئوية. في ظل هذه الظروف ، تكون الأملاح في حالة منصهرة ، وتشكل إلكتروليتًا. عند القطب الموجب ، يتفاعل الهيدروجين مع أيونات ثاني أكسيد الكربون ، مكونًا الماء وثاني أكسيد الكربون وإطلاق الإلكترونات التي يتم إرسالها إلى الدائرة الخارجية ، وفي القطب السالب يتفاعل الأكسجين مع ثاني أكسيد الكربون والإلكترونات من الدائرة الخارجية ، مكونًا أيونات ثاني أكسيد الكربون مرة أخرى.
تم إنشاء عينات مختبرية من خلايا الوقود من هذا النوع في أواخر الخمسينيات من القرن الماضي بواسطة العالمين الهولنديين ج. في الستينيات ، عمل المهندس فرانسيس تي بيكون ، وهو سليل كاتب وعالم إنجليزي شهير من القرن السابع عشر ، على هذه العناصر ، ولهذا السبب يُشار أحيانًا إلى خلايا وقود MCFC باسم عناصر بيكون. استخدمت برامج Apollo و Apollo-Soyuz و Scylab التابعة لوكالة ناسا مثل خلايا الوقود كمصدر للطاقة (الشكل 14). في نفس السنوات ، اختبرت الإدارة العسكرية الأمريكية عدة عينات من خلايا وقود MCFC المصنعة من قبل شركة Texas Instruments ، حيث تم استخدام درجات الجيش من البنزين كوقود. في منتصف السبعينيات ، بدأت وزارة الطاقة الأمريكية البحث لتطوير خلية وقود كربونات منصهرة ثابتة مناسبة لـ تطبيق عملي. في التسعينيات ، تم تشغيل عدد من الوحدات التجارية التي تصل قوتها إلى 250 كيلوواط ، مثل المحطة الجوية البحرية الأمريكية ميرامار في كاليفورنيا. في عام 1996 ، تم إنشاء شركة FuelCell Energy، Inc. بتكليف من 2 ميغاواط مصنع ما قبل السلسلة في سانتا كلارا ، كاليفورنيا.
خلايا وقود أكسيد الحالة الصلبة (SOFC)
تتميز خلايا وقود أكسيد الحالة الصلبة بالبساطة في التصميم وتعمل في درجات حرارة عالية جدًا - 700-1000 درجة مئوية. تسمح درجات الحرارة المرتفعة هذه باستخدام وقود "متسخ" نسبيًا وغير مكرر. تحدد نفس الميزات الموجودة في خلايا الوقود القائمة على الكربونات المنصهرة مجالًا مشابهًا للتطبيق - مصادر ثابتة كبيرة للحرارة والكهرباء.
تختلف خلايا وقود الأكسيد الصلب هيكليًا عن خلايا الوقود المعتمدة على تقنيات PAFC و MCFC. يصنع القطب الموجب والكاثود والإلكتروليت من درجات خاصة من السيراميك. في أغلب الأحيان ، يتم استخدام خليط من أكسيد الزركونيوم وأكسيد الكالسيوم كإلكتروليت ، ولكن يمكن استخدام أكاسيد أخرى. يشكل المنحل بالكهرباء شبكة بلورية مغلفة على كلا الجانبين بمادة قطب مسامية. من الناحية الهيكلية ، تصنع هذه العناصر في شكل أنابيب أو ألواح مسطحة ، مما يجعل من الممكن استخدام التقنيات المستخدمة على نطاق واسع في صناعة الإلكترونيات في تصنيعها. نتيجة لذلك ، يمكن لخلايا وقود أكسيد الحالة الصلبة أن تعمل في درجات حرارة عالية جدًا ، مما يجعلها مفيدة لتوليد الطاقة الكهربائية والحرارية.
في درجات حرارة التشغيل العالية ، تتشكل أيونات الأكسجين عند الكاثود ، والتي تنتقل عبر الشبكة البلورية إلى القطب الموجب ، حيث تتفاعل مع أيونات الهيدروجين ، وتشكل الماء وتطلق الإلكترونات الحرة. في هذه الحالة ، يتم إطلاق الهيدروجين من الغاز الطبيعي مباشرة في الخلية ، أي ليست هناك حاجة لمصلح منفصل.
تم وضع الأسس النظرية لإنشاء خلايا وقود أكسيد الحالة الصلبة في أواخر ثلاثينيات القرن الماضي ، عندما أجرى العلماء السويسريون باور (إميل باور) وبريس (إتش. برييس) تجارب باستخدام الزركونيوم والإيتريوم والسيريوم واللانثانوم والتنغستن ، باستخدامها. كالكهارل.
تم إنشاء النماذج الأولية لخلايا الوقود هذه في أواخر الخمسينيات من القرن الماضي من قبل عدد من الشركات الأمريكية والهولندية. سرعان ما تخلت معظم هذه الشركات عن إجراء المزيد من الأبحاث بسبب الصعوبات التكنولوجية ، ولكن إحداها ، Westinghouse Electric Corp. (الآن "Siemens Westinghouse Power Corporation") ، واصل العمل. تقبل الشركة حاليًا الطلبات المسبقة لنموذج تجاري لخلية وقود أكسيد صلب طوبولوجيا أنبوبي متوقع هذا العام (الشكل 15). جزء السوق من هذه العناصر هو التركيبات الثابتة لإنتاج الحرارة والطاقة الكهربائية بسعة 250 كيلوواط إلى 5 ميغاواط.
أظهرت خلايا الوقود من نوع SOFC موثوقية عالية جدًا. على سبيل المثال ، سجلت خلية وقود نموذجية من شركة سيمنز ويستنجهاوس 16600 ساعة وتستمر في العمل ، مما يجعلها أطول خلية وقود مستمرة في العالم.
يسمح وضع التشغيل ذو درجة الحرارة العالية والضغط العالي لخلايا وقود SOFC بإنشاء محطات هجينة ، حيث تعمل انبعاثات خلايا الوقود على تشغيل توربينات الغاز المستخدمة لتوليد الكهرباء. أول مصنع هجين من هذا القبيل قيد التشغيل في إيرفين ، كاليفورنيا. تبلغ الطاقة المقدرة لهذه المحطة 220 كيلوواط ، منها 200 كيلوواط من خلية الوقود و 20 كيلوواط من مولد التوربينات الصغيرة.
خلية الوقود عبارة عن جهاز تحويل طاقة كهروكيميائية يحول الهيدروجين والأكسجين إلى كهرباء من خلال تفاعل كيميائي. نتيجة لهذه العملية ، يتكون الماء ويتم إطلاق كمية كبيرة من الحرارة. تشبه خلية الوقود إلى حد بعيد البطارية التي يمكن شحنها ثم استخدامها لتخزين الطاقة الكهربائية.
مخترع خلية الوقود هو William R. Grove ، الذي اخترعها مرة أخرى في عام 1839. في خلية الوقود هذه ، تم استخدام محلول حمض الكبريتيك كإلكتروليت ، وتم استخدام الهيدروجين كوقود ، والذي تم دمجه مع الأكسجين في وسط مؤكسد . وتجدر الإشارة إلى أنه حتى وقت قريب ، كانت خلايا الوقود تستخدم فقط في المختبرات وعلى المركبات الفضائية.
في المستقبل ، ستكون خلايا الوقود قادرة على التنافس مع العديد من أنظمة تحويل الطاقة الأخرى (بما في ذلك توربينات الغاز في محطات توليد الطاقة) ، ومحركات الاحتراق الداخلي في السيارات والبطاريات الكهربائية في الأجهزة المحمولة. تعمل محركات الاحتراق الداخلي على حرق الوقود واستخدام الضغط الناتج عن تمدد غازات الاحتراق لأداء الأعمال الميكانيكية. تخزن البطاريات الطاقة الكهربائية ثم تحولها إلى طاقة كيميائية ، والتي يمكن تحويلها مرة أخرى إلى طاقة كهربائية إذا لزم الأمر. من المحتمل أن تكون خلايا الوقود فعالة للغاية. في عام 1824 ، أثبت العالم الفرنسي كارنو أن دورات التمدد الانضغاطي لمحرك الاحتراق الداخلي لا يمكن أن تضمن كفاءة تحويل الطاقة الحرارية (وهي الطاقة الكيميائية لوقود الاحتراق) إلى طاقة ميكانيكية تزيد عن 50٪. لا تحتوي خلية الوقود على أجزاء متحركة (على الأقل ليس داخل الخلية نفسها) ، وبالتالي فهي لا تخضع لقانون كارنو. وبطبيعة الحال ، ستتمتع بكفاءة تزيد عن 50٪ وتكون فعالة بشكل خاص في الأحمال المنخفضة. وبالتالي ، فإن مركبات خلايا الوقود مهيأة لتكون (وقد أثبتت بالفعل أنها) أكثر كفاءة في استهلاك الوقود من المركبات التقليدية في ظروف القيادة الحقيقية.
تولد خلية الوقود تيارًا كهربائيًا مستمرًا يمكن استخدامه لقيادة محرك كهربائي وتركيبات الإضاءة والأنظمة الكهربائية الأخرى في السيارة. هناك عدة أنواع من خلايا الوقود تختلف في العمليات الكيميائية المستخدمة. عادة ما يتم تصنيف خلايا الوقود حسب نوع المنحل بالكهرباء الذي تستخدمه. تعد بعض أنواع خلايا الوقود واعدة لتطبيقات محطات الطاقة ، بينما قد يكون البعض الآخر مفيدًا للأجهزة المحمولة الصغيرة أو لقيادة السيارات.
خلية الوقود القلوية هي واحدة من أقدم العناصر المتقدمة. لقد تم استخدامها من قبل برنامج الفضاء الأمريكي منذ الستينيات. خلايا الوقود هذه معرضة جدًا للتلوث ، وبالتالي تتطلب هيدروجينًا وأكسجينًا نقيًا جدًا. بالإضافة إلى ذلك ، فهي باهظة الثمن ، وبالتالي من غير المرجح أن يجد هذا النوع من خلايا الوقود تطبيقًا واسعًا في السيارات.
يمكن استخدام خلايا الوقود القائمة على حمض الفوسفوريك في التركيبات الثابتة منخفضة الطاقة. تعمل في درجات حرارة عالية إلى حد ما ، وبالتالي تستغرق وقتًا طويلاً لتسخينها ، مما يجعلها أيضًا غير فعالة للاستخدام في السيارات.
خلايا وقود الأكسيد الصلب مناسبة بشكل أفضل لمولدات الطاقة الثابتة الكبيرة التي يمكن أن توفر الكهرباء للمصانع أو المجتمعات. يعمل هذا النوع من خلايا الوقود في درجات حرارة عالية جدًا (حوالي 1000 درجة مئوية). تسبب درجة حرارة التشغيل المرتفعة مشاكل معينة ، ولكن من ناحية أخرى ، هناك ميزة - يمكن إرسال البخار الناتج عن خلية الوقود إلى التوربينات لتوليدها كمية كبيرةكهرباء. بشكل عام ، هذا يحسن الكفاءة الكلية للنظام.
واحدة من أكثر الأنظمة الواعدة هي خلية وقود غشاء تبادل البروتون - POMFC (PEMFC - خلية وقود غشاء تبادل البروتون). في الوقت الحالي ، يعد هذا النوع من خلايا الوقود هو الأكثر واعدة لأنه يمكن أن يدفع السيارات والحافلات والمركبات الأخرى.
العمليات الكيميائية في خلية الوقود
تستخدم خلايا الوقود عملية كهروكيميائية للجمع بين الهيدروجين والأكسجين من الهواء. مثل البطاريات ، تستخدم خلايا الوقود أقطابًا كهربائية (موصلات كهربائية صلبة) في إلكتروليت (وسط موصل كهربائيًا). عندما تتلامس جزيئات الهيدروجين مع القطب السالب (الأنود) ، يتم فصل الأخير إلى بروتونات وإلكترونات. تمر البروتونات عبر غشاء تبادل البروتون (POM) إلى القطب الموجب (الكاثود) لخلية الوقود ، وتنتج الكهرباء. هناك مزيج كيميائي من جزيئات الهيدروجين والأكسجين مع تكوين الماء ، كمنتج ثانوي لهذا التفاعل. النوع الوحيد من الانبعاثات من خلية الوقود هو بخار الماء.
يمكن استخدام الكهرباء التي تنتجها خلايا الوقود في مجموعة نقل الحركة الكهربائية للمركبة (التي تتكون من محول طاقة كهربائية ومحرك تحريضي يعمل بالتيار المتردد) لتوفير الطاقة الميكانيكية لدفع السيارة. تتمثل وظيفة محول الطاقة في تحويل التيار المباشر الناتج عن خلايا الوقود إلى تيار متناوب ، والذي يستخدمه محرك الجر في السيارة.
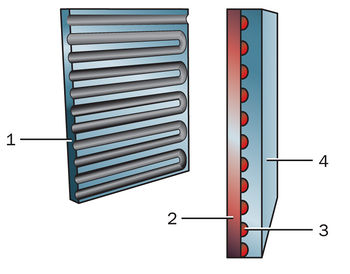
رسم تخطيطي لخلية وقود مع غشاء تبادل البروتون:
1 - الأنود
2 - غشاء تبادل البروتون (REM) ؛
3 - محفز (أحمر) ؛
4 - الكاثود
تستخدم خلية وقود غشاء التبادل البروتوني (PEMFC) أحد أبسط التفاعلات لأي خلية وقود.

خلية وقود منفصلة
ضع في اعتبارك كيف تعمل خلية الوقود. يقوم القطب الموجب ، وهو القطب السالب لخلية الوقود ، بتوصيل الإلكترونات التي يتم تحريرها من جزيئات الهيدروجين بحيث يمكن استخدامها في دائرة كهربائية خارجية (دائرة). للقيام بذلك ، يتم حفر القنوات فيه ، وتوزيع الهيدروجين بالتساوي على كامل سطح المحفز. يحتوي الكاثود (القطب الموجب لخلية الوقود) على قنوات توزع الأكسجين على سطح المحفز. كما أنه يعيد الإلكترونات من الدائرة الخارجية (الدائرة) إلى المحفز ، حيث يمكن أن تتحد مع أيونات الهيدروجين والأكسجين لتكوين الماء. المنحل بالكهرباء عبارة عن غشاء يتبادل البروتونات. هذه مادة خاصة ، شبيهة بالبلاستيك العادي ، ولكن لها القدرة على تمرير أيونات موجبة الشحنة ومنع مرور الإلكترونات.
المحفز عبارة عن مادة خاصة تسهل التفاعل بين الأكسجين والهيدروجين. عادة ما يتم تصنيع المحفز من مسحوق البلاتين المترسب في طبقة رقيقة جدًا على ورق أو قطعة قماش كربون. يجب أن يكون المحفز خشنًا ومساميًا بحيث يمكن أن يتلامس سطحه مع الهيدروجين والأكسجين قدر الإمكان. يقع الجانب المطلي بالبلاتين من المحفز أمام غشاء تبادل البروتون (POM).
يتم توفير غاز الهيدروجين (H 2) لخلية الوقود تحت ضغط من جانب الأنود. عندما يتلامس جزيء H2 مع البلاتين الموجود في المحفز ، فإنه ينقسم إلى جزأين ، أيونين (H +) وإلكترونين (e–). يتم توصيل الإلكترونات من خلال الأنود حيث تمر عبر دائرة خارجية (دائرة) تقوم بعمل مفيد (مثل قيادة محرك كهربائي) والعودة من جانب الكاثود لخلية الوقود.
وفي الوقت نفسه ، من جانب الكاثود لخلية الوقود ، يتم دفع غاز الأكسجين (O 2) عبر المحفز حيث يشكل ذرتين من الأكسجين. كل من هذه الذرات لها شحنة سالبة قوية تجذب اثنين من أيونات H + عبر الغشاء ، حيث تتحد مع ذرة أكسجين وإلكترونين من الحلقة الخارجية (سلسلة) لتكوين جزيء ماء (H 2 O).
ينتج هذا التفاعل في خلية وقود واحدة قوة تقارب 0.7 واط. من أجل رفع الطاقة إلى المستوى المطلوب ، من الضروري دمج العديد من خلايا الوقود الفردية لتشكيل مجموعة خلايا وقود.
تعمل خلايا الوقود POM عند درجة حرارة منخفضة نسبيًا (حوالي 80 درجة مئوية) ، مما يعني أنه يمكن تسخينها بسرعة إلى درجة حرارة التشغيل ولا تتطلب أنظمة تبريد باهظة الثمن. أدى التحسين المستمر في التكنولوجيا والمواد المستخدمة في هذه الخلايا إلى جعل قوتها أقرب إلى المستوى الذي يمكن أن توفر فيه بطارية من خلايا الوقود هذه ، التي تشغل جزءًا صغيرًا من صندوق السيارة ، الطاقة اللازمة لقيادة السيارة.
على مدى السنوات الماضية ، استثمر معظم مصنعي السيارات الرائدين في العالم بشكل كبير في تطوير تصميمات السيارات باستخدام خلايا الوقود. لقد أظهر الكثيرون بالفعل مركبات تعمل بخلايا الوقود ذات قوة وخصائص ديناميكية مرضية ، على الرغم من أنها كانت باهظة الثمن.
تحسين تصميم هذه السيارات مكثف للغاية.

مركبة تعمل بخلايا الوقود ، تستخدم محطة طاقة تقع تحت أرضية السيارة
تعتمد مركبة NECAR V على سيارة Mercedes-Benz A-class ، مع محطة الطاقة بالكامل ، جنبًا إلى جنب مع خلايا الوقود ، الموجودة أسفل أرضية السيارة. مثل هذا الحل البناء يجعل من الممكن استيعاب أربعة ركاب وأمتعة في السيارة. هنا ، ليس الهيدروجين ، لكن الميثانول يستخدم كوقود للسيارة. يتم تحويل الميثانول بمساعدة مصلح (جهاز يحول الميثانول إلى هيدروجين) إلى هيدروجين ، وهو أمر ضروري لتشغيل خلية الوقود. يتيح استخدام المصلح على متن السيارة إمكانية استخدام أي هيدروكربون تقريبًا كوقود ، مما يجعل من الممكن إعادة التزود بالوقود في سيارة تعمل بخلايا الوقود باستخدام شبكة محطات الوقود الحالية. من الناحية النظرية ، لا تنتج خلايا الوقود شيئًا سوى الكهرباء والماء. إن تحويل الوقود (البنزين أو الميثانول) إلى الهيدروجين المطلوب لخلية الوقود يقلل إلى حد ما من الجاذبية البيئية لمثل هذه السيارة.
أنتجت هوندا ، التي تعمل في مجال خلايا الوقود منذ عام 1989 ، مجموعة صغيرة من سيارات هوندا FCX-V4 في عام 2003 بخلايا وقود تبادل البروتونات. نوع الغشاءشركة بالارد. تولد خلايا الوقود هذه 78 كيلوواط من الطاقة الكهربائية ، وتستخدم محركات الجر بقوة 60 كيلوواط وعزم الدوران 272 نيوتن متر لقيادة عجلات القيادة.لديها ديناميكيات ممتازة ، كما أن إمداد الهيدروجين المضغوط يجعل من الممكن تشغيلها تصل إلى 355 كم.

تستخدم Honda FCX طاقة خلايا الوقود لدفع نفسها.
هوندا FCX هي أول سيارة تعمل بخلايا الوقود في العالم تحصل على شهادة حكومية في الولايات المتحدة. السيارة حاصلة على شهادة ZEV - سيارة خالية من الانبعاثات (خالية من التلوث). لن تبيع هوندا هذه السيارات بعد ، لكنها تستأجر حوالي 30 سيارة لكل وحدة. كاليفورنيا وطوكيو ، حيث توجد بالفعل بنية تحتية لتزويد وقود الهيدروجين.
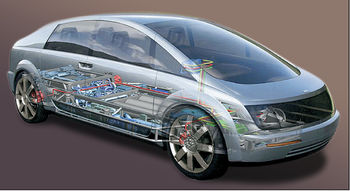
تحتوي السيارة الاختبارية Hy Wire من جنرال موتورز على محطة طاقة تعمل بخلايا الوقود
تجري جنرال موتورز بحثًا كبيرًا حول تطوير وإنشاء مركبات تعمل بخلايا الوقود.

هيكل السيارة هاي واير
حصلت السيارة الاختبارية GM Hy Wire على 26 براءة اختراع. أساس السيارة عبارة عن منصة وظيفية بسمك 150 مم. داخل المنصة توجد اسطوانات الهيدروجين ومحطة طاقة تعمل بخلايا الوقود وأنظمة التحكم في السيارة باستخدام أحدث التكنولوجياالتحكم الإلكتروني بالأسلاك. هيكل سيارة Hy Wire عبارة عن منصة رفيعة تحيط بكل شيء العناصر الأساسيةهياكل المركبات: اسطوانات الهيدروجين وخلايا الوقود والبطاريات والمحركات الكهربائية وأنظمة التحكم. هذا النهج في التصميم يجعل من الممكن تغيير أجسام السيارات أثناء التشغيل ، كما تقوم الشركة باختبار مركبات خلايا الوقود التجريبية أوبل وتصميم مصنع لإنتاج خلايا الوقود.
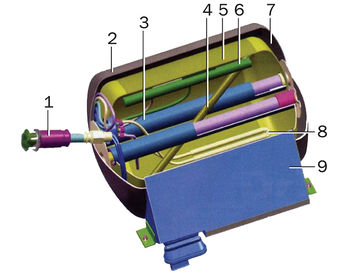
تصميم خزان وقود "آمن" للهيدروجين المسال:
1 - جهاز التعبئة ؛
2 - الخزان الخارجي ؛
3 - يدعم
4 - مستشعر المستوى
5 - خزان داخلي ؛
6 - خط التعبئة ؛
7 - العزلة والفراغ.
8 - سخان
9 - صندوق التثبيت
تولي شركة BMW اهتمامًا كبيرًا لمشكلة استخدام الهيدروجين كوقود للسيارات. بالتعاون مع Magna Steyer ، المشهورة بعملها على استخدام الهيدروجين المسال في أبحاث الفضاء ، طورت BMW خزان وقود الهيدروجين المسال الذي يمكن استخدامه في السيارات.

أكدت الاختبارات سلامة استخدام خزان وقود بهيدروجين سائل
أجرت الشركة سلسلة من الاختبارات على سلامة الهيكل وفق الأساليب المعيارية وأكدت موثوقيتها.
في عام 2002 ، في معرض فرانكفورت للسيارات (ألمانيا) ، تم عرض ميني كوبر هيدروجين ، والذي يستخدم الهيدروجين المسال كوقود. خزان الوقودتشغل هذه السيارة نفس مساحة خزان الغاز التقليدي. لا يستخدم الهيدروجين في هذه السيارة لخلايا الوقود ، بل يستخدم كوقود لمحركات الاحتراق الداخلي.

أول سيارة في العالم يتم إنتاجها بكميات كبيرة بخلية وقود بدلاً من بطارية
في عام 2003 ، أعلنت شركة BMW عن إطلاق أول سيارة تعمل بخلايا الوقود ذات الإنتاج الضخم ، وهي BMW 750 hL. يتم استخدام بطارية خلايا الوقود بدلاً من البطارية التقليدية. تحتوي هذه السيارة على محرك احتراق داخلي مكون من 12 أسطوانة يعمل بالهيدروجين ، وتعمل خلية الوقود كبديل للبطارية التقليدية ، مما يسمح لمكيف الهواء والمستهلكين الآخرين بالعمل عندما تكون السيارة متوقفة لفترة طويلة مع إيقاف تشغيل المحرك.

يتم إعادة التزود بالوقود بالهيدروجين بواسطة روبوت ، ولا يشارك السائق في هذه العملية
قامت نفس الشركة BMW أيضًا بتطوير موزعات وقود آلية توفر إعادة التزود بالوقود بشكل سريع وآمن للسيارات باستخدام الهيدروجين المسال.
يشير ظهور عدد كبير من التطورات في السنوات الأخيرة بهدف إنشاء مركبات تستخدم أنواعًا بديلة من الوقود ومحطات الطاقة البديلة إلى أن محركات الاحتراق الداخلي ، التي هيمنت على السيارات خلال القرن الماضي ، ستفسح المجال في النهاية لتصميمات أنظف وأكثر كفاءة وصامتة. استخدامها على نطاق واسع في الوقت الحاضر لا تتراجع بسبب المشاكل التقنية ، ولكن بالأحرى من المشاكل الاقتصادية والاجتماعية. لاستخدامها على نطاق واسع ، من الضروري إنشاء بنية تحتية معينة لتطوير الإنتاج الأنواع البديلةالوقود ، وإنشاء وتوزيع محطات وقود جديدة وتذليل عدد من الحواجز النفسية. سيتطلب استخدام الهيدروجين كوقود للمركبة معالجة قضايا التخزين والتسليم والتوزيع ، مع اتخاذ تدابير سلامة جادة.
من الناحية النظرية ، يتوفر الهيدروجين بكميات غير محدودة ، لكن إنتاجه كثيف للغاية للطاقة. بالإضافة إلى ذلك ، من أجل تحويل السيارات للعمل على وقود الهيدروجين ، يجب إجراء تغييرين كبيرين في نظام الطاقة: أولاً ، نقل تشغيلها من البنزين إلى الميثانول ، ثم إلى الهيدروجين لبعض الوقت. سوف يمر بعض الوقت قبل أن يتم حل هذه المشكلة.
خلية وقود الهيدروجين في نيسان
تتحسن الإلكترونيات المحمولة كل عام ، وتصبح أكثر انتشارًا ويمكن الوصول إليها: أجهزة المساعد الرقمي الشخصي ، وأجهزة الكمبيوتر المحمولة ، والأجهزة المحمولة والرقمية ، وإطارات الصور ، وما إلى ذلك ، يتم تحديثها جميعًا باستمرار بميزات جديدة ، وشاشات أكبر ، واتصالات لاسلكية ، ومعالجات أقوى ، مع انخفاض في الحجم. تقنيات الطاقة ، على عكس تكنولوجيا أشباه الموصلات ، لا تسير بسرعة فائقة.
أصبحت البطاريات والمراكم المتاحة لتشغيل إنجازات الصناعة غير كافية ، وبالتالي فإن مسألة المصادر البديلة حادة للغاية. خلايا الوقود هي إلى حد بعيد الاتجاه الواعد. تم اكتشاف مبدأ تشغيلهم مرة أخرى في عام 1839 من قبل ويليام جروف ، الذي قام بتوليد الكهرباء عن طريق تغيير التحليل الكهربائي للماء.
ما هي خلايا الوقود؟
فيديو: وثائقي ، خلايا الوقود للنقل: الماضي ، الحاضر ، المستقبل
خلايا الوقود تهم مصنعي السيارات ، كما يهتم صانعو المركبات الفضائية بها. في عام 1965 ، تم اختبارهم حتى من قبل أمريكا على الجوزاء 5 التي تم إطلاقها في الفضاء ، وبعد ذلك على أبولو. يتم استثمار ملايين الدولارات في أبحاث خلايا الوقود اليوم مع مخاوف التلوث بيئة، زيادة انبعاثات غازات الاحتباس الحراري الناتجة عن احتراق الوقود الأحفوري ، والتي لا تعد احتياطياتها أيضًا بلا حدود.
تعمل خلية الوقود ، التي يشار إليها غالبًا باسم المولد الكهروكيميائي ، بالطريقة الموضحة أدناه.
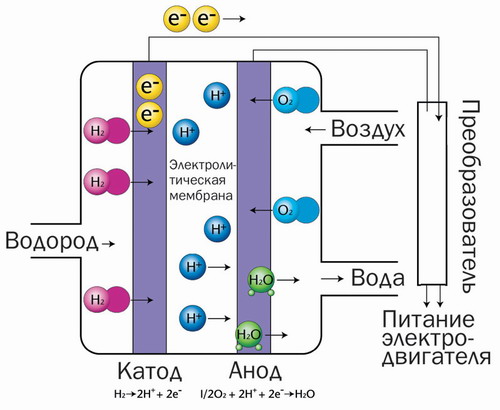
كونها ، مثل البطاريات والمراكم ، خلية كلفانية ، ولكن مع اختلاف المواد الفعالة يتم تخزينها فيها بشكل منفصل. يأتون إلى الأقطاب الكهربائية عند استخدامها. يحترق الوقود الطبيعي أو أي مادة يتم الحصول عليها منه على القطب السالب ، والذي يمكن أن يكون غازيًا (الهيدروجين ، على سبيل المثال ، وأول أكسيد الكربون) أو سائل ، مثل الكحول. في القطب الموجب ، كقاعدة عامة ، يتفاعل الأكسجين.
لكن ليس من السهل ترجمة مبدأ العمل البسيط المظهر إلى واقع.
خلية وقود DIY
فيديو: خلية وقود الهيدروجين DIY
لسوء الحظ ، ليس لدينا صور لما يجب أن يبدو عليه عنصر الوقود هذا ، نأمل أن تكون خيالك.
يمكن صنع خلية وقود منخفضة الطاقة بيديك حتى في مختبر المدرسة. من الضروري تخزين قناع غاز قديم وعدة قطع من زجاج شبكي وقلوي ومحلول مائي من كحول الإيثيل (ببساطة أكثر ، الفودكا) ، والذي سيكون بمثابة "وقود" لخلية الوقود.

بادئ ذي بدء ، أنت بحاجة إلى مبيت لخلية الوقود ، وهو الأفضل مصنوعًا من زجاج شبكي ، بسمك لا يقل عن خمسة ملليمترات. يمكن جعل الأقسام الداخلية (خمس حجرات بالداخل) أرق قليلاً - 3 سم. بالنسبة للالتصاق بالزجاج الشبكي ، يتم استخدام غراء التركيب التالي: يتم إذابة ستة جرامات من رقائق زجاج شبكي في مائة جرام من الكلوروفورم أو ثنائي كلورو الإيثان (تعمل تحت غطاء محرك السيارة ).
في الجدار الخارجي ، من الضروري الآن حفر حفرة تحتاج فيها إلى إدخال أنبوب زجاجي للتصريف بقطر 5-6 سم من خلال سدادة مطاطية.
يعلم الجميع أنه في الجدول الدوري في الزاوية اليسرى السفلية توجد المعادن الأكثر نشاطًا ، وتوجد المعادن ذات النشاط العالي في الجدول في الزاوية اليمنى العليا ، أي تزداد القدرة على التبرع بالإلكترونات من أعلى إلى أسفل ومن اليمين إلى اليسار. العناصر التي ، في ظل ظروف معينة ، يمكن أن تظهر على شكل معادن أو أشباه فلزات موجودة في وسط الجدول.
الآن ، في الجزأين الثاني والرابع ، نسكب الكربون المنشط من قناع الغاز (بين القسم الأول والثاني ، وكذلك الثالث والرابع) ، والذي سيكون بمثابة أقطاب كهربائية. حتى لا ينسكب الفحم من خلال الفتحات ، يمكن وضعه في قماش نايلون (ستعمل جوارب النايلون النسائية). في
سوف يتم تداول الوقود في الغرفة الأولى ، في الغرفة الخامسة يجب أن يكون هناك مورد أكسجين - الهواء. سيكون هناك إلكتروليت بين الأقطاب الكهربائية ، ومن أجل منعه من التسرب إلى غرفة الهواء ، من الضروري نقعه بمحلول من البارافين في البنزين (نسبة 2 جرام من البارافين إلى نصف كوب من البنزين) قبل ملء الحجرة الرابعة بالفحم لإلكتروليت الهواء. على طبقة من الفحم ، تحتاج إلى وضع ألواح نحاسية (ضاغطة قليلاً) ، والتي يتم لحام الأسلاك بها. من خلالهم ، سيتم تحويل التيار من الأقطاب الكهربائية.
يبقى فقط لشحن العنصر. لهذا ، هناك حاجة إلى الفودكا ، والتي يجب تخفيفها بالماء في 1: 1. ثم أضف بعناية ثلاثمائة إلى ثلاثمائة وخمسين جرامًا من البوتاسيوم الكاوية. بالنسبة للكهارل ، يتم إذابة 70 جرامًا من البوتاسيوم الكاوية في 200 جرام من الماء.
خلية الوقود جاهزة للاختبار.أنت الآن بحاجة إلى صب الوقود في نفس الوقت في الحجرة الأولى ، والإلكتروليت في الغرفة الثالثة. يجب أن يظهر مقياس الفولتميتر المتصل بالأقطاب الكهربائية من 07 فولت إلى 0.9. لضمان التشغيل المستمر للعنصر ، من الضروري تصريف الوقود المستهلك (تصريفه في كوب) وإضافة وقود جديد (من خلال أنبوب مطاطي). يتم التحكم في معدل التغذية عن طريق ضغط الأنبوب. هذه هي الطريقة التي يبدو بها تشغيل خلية الوقود في ظروف المختبر ، والتي تكون قوتها صغيرة بشكل مفهوم.
فيديو: خلية وقود أو بطارية أبدية في المنزل
لجعل القوة أكبر ، عمل العلماء على هذه المشكلة لفترة طويلة. توجد خلايا وقود الميثانول والإيثانول على فولاذ التطوير النشط. ولكن ، للأسف ، لا توجد طريقة حتى الآن لتطبيقها.
لماذا يتم اختيار خلية الوقود كمصدر بديل للطاقة

تم اختيار خلية وقود كمصدر طاقة بديل ، لأن المنتج النهائي لاحتراق الهيدروجين فيه هو الماء. المشكلة هي فقط في العثور على غير مكلفة و على نحو فعالالحصول على الهيدروجين. الأموال الضخمة المستثمرة في تطوير مولدات الهيدروجين وخلايا الوقود لا يمكن أن تفشل في أن تؤتي ثمارها ، وبالتالي فإن الاختراق التكنولوجي واستخدامهم الحقيقي في الحياة اليومية، فقط مسألة وقت.
اليوم بالفعل وحوش صناعة السيارات:تعرض جنرال موتورز وهوندا ودريملر كويسلر وبالارد حافلات وسيارات تعمل بخلايا وقود بقوة تصل إلى 50 كيلو واط. لكن المشكلات المرتبطة بسلامتها وموثوقيتها وتكلفتها - لم يتم حلها بعد. كما ذكرنا سابقًا ، على عكس مصادر الطاقة التقليدية - البطاريات والبطاريات ، في هذه الحالة ، يتم توفير المؤكسد والوقود من الخارج ، وتكون خلية الوقود مجرد وسيط في التفاعل المستمر لحرق الوقود وتحويل الطاقة المنبعثة إلى كهرباء . يحدث "الاحتراق" فقط إذا أعطى العنصر تيارًا للحمل ، مثل مولد كهربائي يعمل بالديزل ، ولكن بدون مولد وديزل ، وأيضًا بدون ضوضاء ودخان وسخونة زائدة. في الوقت نفسه ، تكون الكفاءة أعلى بكثير ، حيث لا توجد آليات وسيطة.
فيديو: سيارة تعمل بخلايا وقود الهيدروجين
يتم وضع آمال كبيرة على استخدام التقنيات النانوية والمواد النانوية، مما سيساعد على تصغير خلايا الوقود ، مع زيادة قوتها. كانت هناك تقارير تفيد بأنه تم إنشاء محفزات فائقة الكفاءة ، بالإضافة إلى تصميمات خلايا الوقود التي لا تحتوي على أغشية. في نفوسهم ، جنبًا إلى جنب مع المؤكسد ، يتم توفير الوقود (الميثان ، على سبيل المثال) إلى العنصر. الحلول مثيرة للاهتمام ، حيث يتم استخدام الأكسجين المذاب في الماء كعامل مؤكسد ، والشوائب العضوية المتراكمة في المياه الملوثة تستخدم كوقود. هذه هي خلايا الوقود الحيوي المزعومة.
خلايا الوقود ، وفقًا للخبراء ، يمكن أن تدخل السوق الشامل في السنوات القادمة